在2NO+O2 2NO2(正反应为吸热反应)中,下列表明在30 ℃和100 ℃时平衡体系中,NO的百分含量与压强(p)或压强一定时与时间的关系图象,正确的是( )
2NO2(正反应为吸热反应)中,下列表明在30 ℃和100 ℃时平衡体系中,NO的百分含量与压强(p)或压强一定时与时间的关系图象,正确的是( )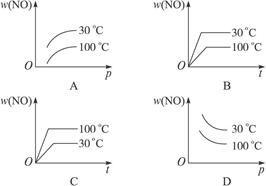
在下列有FeCl3溶液参加的反应中,与Fe3+水解有关的反应是
①FeCl3溶液与Cu的反应②将FeCl3溶液加热蒸干,并灼烧最终得到Fe2O3③饱和FeCl3溶液滴入沸水中制备Fe(OH)3胶体④配制FeCl3溶液需加入一定量的盐酸
| A.①④ | B.②③④ | C.②③ | D.①②③④ |
不能说明CH3COOH是弱酸的事实是
| A.醋酸钠溶液显碱性 |
B.10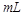 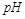 =2的醋酸溶液加水稀释到100 =2的醋酸溶液加水稀释到100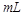 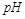 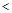 3 3 |
C.中和10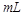 0.1 0.1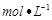 醋酸溶液,需要消耗0.1 醋酸溶液,需要消耗0.1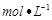 氢氧化钠溶液10 氢氧化钠溶液10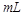 |
| D.0.1 mol·L-1的醋酸溶液中,氢离子浓度约为0.001 mol·L-1 |
下列离子方程式书写正确的是
A.NaHS水解反应:HS-+ H2O   H3O++ S2- H3O++ S2- |
B.明矾加入在水中起净化作用的原因:Al3++ 3H2O 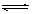 Al(OH)3(胶体) + 3H+ Al(OH)3(胶体) + 3H+ |
C.氢氧化钡溶液与稀硫酸反应:Ba2++SO 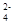 +H++OH-===BaSO4↓+H2O +H++OH-===BaSO4↓+H2O |
| D.碳酸氢钠溶液中加入过量Ba(OH)2溶液: |
2HCO3- + Ba2+ + 2OH-= BaCO3↓+ CO32-+ 2H2O
关于强、弱电解质的叙述不正确的是( )
| A.强电解质在溶液中完全电离成阴、阳离子 |
| B.强电解质溶液导电能力不一定比弱电解质溶液导电能力强 |
| C.同一弱电解质同浓度的溶液,温度不同时,导电能力不同 |
| D.强电解质易溶于水,弱电解质一定难溶于水 |
下列说法中正确的是( )
| A.0.1 mol∙L−1NH4Cl溶液的KW大于0.01mol∙L−1NH4Cl溶液的KW |
| B.当镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
C.N2(g)+3H2(g) 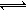 2NH3(g) △H<0,其他条件不变时,升高温度,反应速率v(H2)和H2的平衡转化率α(H2)均增大 2NH3(g) △H<0,其他条件不变时,升高温度,反应速率v(H2)和H2的平衡转化率α(H2)均增大 |
| D.水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应 |