实验是化学研究的基础,下图中所示的实验方法、装置或操作完全正确的是( )
已知:氯气不溶于饱和食盐水 

| A.除去混有的杂质气体 | B.浓硫酸稀释  |
| C.分离出AgNO3溶液中的AgCl | D.称量30.46g的NaOH固体 |
在容积可变的密闭容器中存在如下反应:CO(g)+H2O(g)  CO2(g)+H2(g) ΔH<0,下列对图像的分析中不正确的是()
CO2(g)+H2(g) ΔH<0,下列对图像的分析中不正确的是()
| A.图Ⅰ研究的是t0时升高温度对反应速率的影响 |
| B.图Ⅱ研究的是t0时增大压强(缩小体积)或使用催化剂对反应速率的影响 |
| C.图Ⅲ研究的是催化剂对化学平衡的影响,且甲使用了催化剂 |
| D.图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 |
已知:(1)Zn(s)+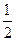 O2(g)===ZnO(s),ΔH1= -348.3 kJ·mol-1,
O2(g)===ZnO(s),ΔH1= -348.3 kJ·mol-1,
(2)2Ag(s)+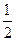 O2(g)===Ag2O(s),ΔH2=-31.0 kJ·mol-1,
O2(g)===Ag2O(s),ΔH2=-31.0 kJ·mol-1,
则Zn(s)+ Ag2O(s)===ZnO(s)+ 2Ag(s)的ΔH等于( )
| A.-379.3 kJ·mol-1 | B.-317.3 kJ·mol-1 |
| C.-332.8 kJ·mol-1 | D.317.3 kJ·mol-1 |
已知肼(N2H4)的燃烧热是534 kJ·mol-1,当它氧化生成1g水时,反应放出的热约为
| A.29.7 kJ | B.14.8 kJ | C.-29.7 kJ/mol | D.-14.8kJ/mol |
已知:CH3COOH(aq)+ NaOH(aq)= CH3COONa(aq)+ H2O(1)△H=-Q1kJ/mol
1/2 H2SO4(浓)+ NaOH(aq)=1/2 Na2SO4(aq) + H2O(1)△H=-Q2kJ/mol
HNO3(aq) + KOH(aq)= KNO3(aq) + H2O(1)△H=-Q3kJ/mol
上述反应均为溶液中的反应,则Q1、Q2、Q3的大小关系为( )
| A.Q2=Q3 > Q1 | B.Q2 > Q1 > Q3 | C.Q2 > Q3 > Q1 | D.Q3 > Q2 > Q1 |
NA表示阿伏加德罗常数。下列说法中,正确的是
A.标准状况下,H2和O2各11.2L相混合,混合气体所含分子总数为NA |
B.1.8g的NH4+中,所含电子总数为NA |
C.14g乙烯和丙烯的混合物中,所含分子总数为3NA |
D.1 mol·L-1的NaOH溶液中,所含Na+总数为NA |