有A,B,C,D,E五种短周期元素,A与B可形成BA型化合物,且A元素是非金属性最强的元素.金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8个;C元素有三种同位素C1,C2,C3,自然界里含最多的是C1,C3的质量数是C1的3倍,C2的原子的质量数是C1的2倍.D的气态氢化物的水溶液呈碱性,而其最高价氧化物的水化物为强酸,E元素原子的最外层电子数比次外层电子数多4个,E离子的核外电子数比质子数多2个.
(1)写出元素名称:A. B. C. D . E. .
(2)写出C1,C2, C3粒子的符号: , ,
(3)写出E离子的结构示意图 E的氢化物的分子式 .
(4)写出A的单质与B的单质反应的化学方程式 ;
(5)写出A的单质和B的单质分别与水反应的化学方程式 , ,将二者反应后生成的溶液混合,发生反应的离子方程式为
(6)A与C形成的化合物中含化学键类型是 .用电子式表示该化合物的形成过程 .
(8分)(1)下图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:_________________ 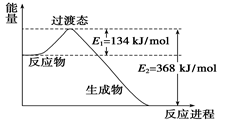
(2)我国实施“嫦娥探月”行动的长征火箭中使用偏二甲肼[(CH3)2N—NH2]作为燃料,其与过氧化氢发生反应放出大量热量C2H8N2(l)+8H2O2(l)===N2(g)+2CO2(g)+12H2O(g) ΔH=-2 500 kJ/mol。如果1 mol偏二甲肼与过氧化氢发生上述反应生成液态水,则反应中放出的热量Q______2 500 kJ(填“<”、“>”或“=”)。
(3)恒温恒容下,2 mol H2与2 mol N2反应达到平衡时,N2为1.8 mol,H2的转化率为________;若该反应在恒温恒压条件下进行(其他条件相同),反应达平衡时,H2的转化率比上述条件下H2的转化率________(填“大”、“小”或“相等”)。
冰毒(化学名:甲基苯丙胺。苯环上有1个取代基)属于芳香族化合物,分子中只含有碳、氢、氮3种元素,相对分子质量不超过150,碳 元素和氢元素质量分数之和为90.6%。请按要求填空:
元素和氢元素质量分数之和为90.6%。请按要求填空:
(1)冰毒的摩尔质量为:_______________ _____;分子式为:____________________。
_____;分子式为:____________________。
(2)冰毒的同分异构体有很多,写出同时符合下列三项要求的冰毒同分异构体的结构简式
______________________________、______________________________(写出其中的2种)
①苯环上只含有两个相邻的取代基
②分子中含有氨基(-NH2)
③分子中含有两个甲基(-CH3)
异丙苯(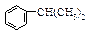 ),是一种重要的有机化工原料。根据题意完成下列填空:
),是一种重要的有机化工原料。根据题意完成下列填空:
(1)由苯与2-丙醇反应制备异丙苯属于__________反应;由异丙苯制备对溴异丙苯的反应试剂和反应条件 为__________________________________________________。
为__________________________________________________。
(2)异丙苯有多种同分异构体,其中一溴代物最少的芳香烃的结构简式是
______________________________。
(3)α-甲基苯乙烯(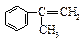 )是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到。写出由异丙苯制取该单体的化学反应方程式:
)是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到。写出由异丙苯制取该单体的化学反应方程式:
_________________ ____________________________________________________________。
____________________________________________________________。
(4)耐热型ABS树脂由丙烯腈(CH2=CHCN)、1,3-丁二烯和α-甲基苯乙烯1∶1∶1共聚生成,写出该树脂的结构简式______________________________。
一种烃的碳架呈三棱柱体(如图所示)
(1)写出该烃的分子式___ _______。
_______。
(2)该烃的一氯取代物有__________种。
(3)该烃的二氯取代物有__________种。
(4)该烃的同分异构体有多种,其中1种不能使酸性高锰酸钾溶液或Br2-CCl4溶液褪色,但在一定条件下能跟溴(或H2)发生取代(或加成)反应,这种同分异构体的结构简式是
____________________。
写出下列反应的化学方程式,注明反应类型:
(1)苯与浓硝酸、浓硫酸的混合物反应(60℃):___________________________________;
(2)甲苯制备 三硝基甲苯:_____________________________________________________;
三硝基甲苯:_____________________________________________________;
(3)乙烯与苯反应:__________________ ______________________________________;
______________________________________;
(4)丙烯与水反应生成醇(主要反应):__________________________________________;
反应类型依次是:____________________________________________________________。