某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证 卤族元素性质的递变规律。图2中A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。
(1)甲同学设计实验的依据是_____________________________________________;
写出选用物质的名称:A____________,B__________,C____________;
(2)甲同学设计的实验中所涉及反应的离子方程式分别为___________________________________________________;
________________________________________________________________________。
(3)乙同学的实验原理是______________________________________________ 。
写出B处的离子方程式: ___________________________________________________。
I.(4分)某温度下的溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L。x与y的关系如图所示:
(1)该温度下,中性溶液的pH=。
(2)该温度下0.01 mol/L NaOH溶液的pH=。
II. (6分)某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
(1)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
| 温度(℃) |
15.0 |
20.0 |
25.0 |
30.0 |
35.0 |
| 平衡总压强(kPa) |
5.7 |
8.3 |
12.0 |
17.1 |
24.0 |
| 平衡气体总浓度 (×10-3mol/L) |
2.4 |
3.4 |
4.8 |
6.8 |
9.4 |
①可以判断该分解反应已经达到化学平衡的是(填字母)。
A.2v(NH3)=v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,计算25.0℃时的分解平衡常数为。
(2)已知:NH2COONH4+2H2O NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。
NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。
③计算25℃时,0~6min氨基甲酸铵水解反应的平均速率为。
④根据图中信息,如何说明水解反应的平均速率随温度升高而增大:
。
某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
实验一配制一定物质的量浓度的醋酸溶液
取冰醋酸配制250mL 0.2000mol/L的醋酸溶液,需要用到的玻璃仪器有量筒、烧杯、玻璃棒、和。
实验二探究浓度对醋酸电离程度的影响
将0.2000mol/L的醋酸溶液稀释成所需浓度的溶液,再用pH计测定25℃时不同浓度的醋酸的pH,结果如下:
| 醋酸浓度(mol/L) |
0.0010 |
0.0100 |
0.0200 |
0.1000 |
0.2000 |
| pH |
3.88 |
3.38 |
3.23 |
2.88 |
2.73 |
回答下列问题:
(1)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是
。
(2)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度
。(填“增大”“减小”或“不变”)
实验室常用的几种气体发生装置如图A、B、C所示: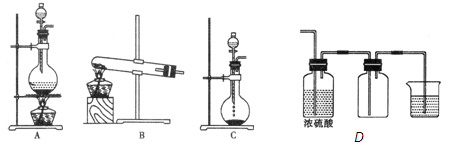
(1)实验室可以用B或C装置制取氨气,如果用C装置,通常使用的药品是。检查C装置气密性是否良好的操作方法是。
(2)气体的性质是气体收集方法选择的主要依据。下列性质与收集方法无关的是(填序号,下同。)
①密度②颜色③溶解性④热稳定性⑤与氧气反应
下图是某学生设计收集气体的几种装置,其中不可行的是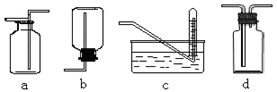
(3)若用A装置与D装置相连制取收集X气体,则X可能是下列气体中的_______
①CO2② NO③ Cl2④H2
其中在D装置中连接小烧杯的目的是________________________。
(共10分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,反应方程式为2NH3+3CuO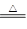 N2+3H2O+3Cu,用示意图中的装置可以实现该反应。回答下列问题:
N2+3H2O+3Cu,用示意图中的装置可以实现该反应。回答下列问题: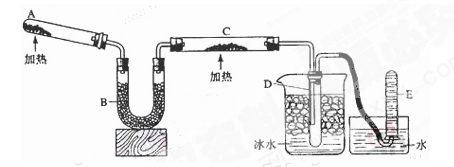
(1)A中发生反应的化学方程式是。检验氨气通常采用的方法及现象是_______________,。
(2)B中加入的物质是,其作用是。
(3)实验时C中观察到的现象是,该反应中氨的作用是_______剂。
(4)若要检验反应生成的水,可将试管D及烧杯部分改成两个相连的干燥管,第一个干燥管X内装有_____________,现象是___________________;第二个干燥管Y内装有碱石灰,作用是____________________________。
某研究性学习小组为研究铁粉与浓硫酸反应所生成气体的成份并测定各气体的含量,进行了如下实验:
【实验推测】足量的铁粉与浓硫酸反应能生成SO2和H2两种气体。
(1)该小组作出此推测的理由是:。
【实验准备】a.供选择的药品:铁粉、浓硫酸、氧化铜粉末、0.2 mol/L的H2C2O4标准溶液、0.1 mol/L的酸性KMnO4标准溶液、酸碱指示剂。
b.实验装置设计及组装(加热及夹持装置均已略去)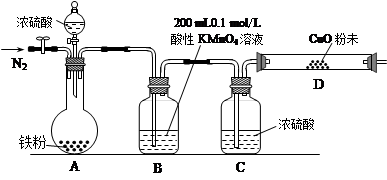
【实验过程及数据处理】
(2)B中发生反应的离子方程式为:。
(3)实验前先通入一段时间的N2,其目的是。
(4)B、C、D中所盛试剂均足量,则证实生成的气体中同时存在SO2和H2的现象是
。
(5)A中反应结束后,继续通N2使A中生成的气体全部赶出,待B、D中反应完全后,先后三次取用B中反应后的溶液于锥形瓶中,每次取用25 mL,用H2C2O4标准溶液进行滴定。
①H2C2O4标准溶液与酸性KMnO4溶液反应的离子方程式如下,请将该方程式完成并配平。
( )H2C2O4+( )MnO4- +( )H+ =( )Mn2+ +( ) H2O+( ) ( )
②滴定达到终点时的现象是。
③重复滴定两次,平均每次耗用H2C2O4标准溶液15.63 mL,则铁与浓硫酸反应产生的SO2气体的物质的量为;经称量,实验前后装置D的质量减少0.9 g,则产生的气体中SO2的体积分数为。