I.(4分)某温度下的溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L。x与y的关系如图所示:
(1)该温度下,中性溶液的pH= 。
(2)该温度下0.01 mol/L NaOH溶液的pH= 。
II. (6分)某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
(1)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
| 温度(℃) |
15.0 |
20.0 |
25.0 |
30.0 |
35.0 |
| 平衡总压强(kPa) |
5.7 |
8.3 |
12.0 |
17.1 |
24.0 |
| 平衡气体总浓度 (×10-3mol/L) |
2.4 |
3.4 |
4.8 |
6.8 |
9.4 |
①可以判断该分解反应已经达到化学平衡的是 (填字母)。
A.2v(NH3)=v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,计算25.0℃时的分解平衡常数为 。
(2)已知:NH2COONH4+2H2O NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。
NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。
③计算25℃时,0~6min氨基甲酸铵水解反应的平均速率为 。
④根据图中信息,如何说明水解反应的平均速率随温度升高而增大:
。
由正丁醇(用nC4H9OH表示)制备正溴丁烷(沸点:101.6 ℃)的反应如下:nC4H9OH+NaBr+H2SO4―→nC4H9Br+NaHSO4+H2O
副反应:nC4H9OH CH3CH2CHCH2↑+H2O
CH3CH2CHCH2↑+H2O
2nC4H9OH (nC4H9)2O+H2O
(nC4H9)2O+H2O
3H2SO4(浓)+2NaBr(固)=2NaHSO4+Br2↑+SO2↑+2H2O
已知反应物及其用量:固体NaBr 0.24 mol,nC4H9OH 0.20 mol,浓H2SO4 29 mL,H2O 20 mL。
制备过程经历如下五个步骤,试回答下列问题:
(1)投料:在圆底烧瓶中加入20 mL水,再慢慢加入29 mL浓硫酸,混合均匀并冷却至室温后,再依次加入0.20 mol正丁醇(约18 mL)和0.24 mol溴化钠,充分振荡后加入几粒沸石。
①冷却至室温后再加正丁醇和溴化钠的目的是________。
| A.减少HBr的挥发 |
| B.防止正丁醇的挥发 |
| C.防止溴化钠被氧化 |
| D.防止温度过高导致炭化结焦 |
②本反应中硫酸与溴化钠作用生成氢溴酸,氢溴酸与正丁醇作用发生取代反应生成正溴丁烷。硫酸的用量和浓度过大都对本制备不利的主要原因是
_____________________________________________________。
(2)加热回流:反应装置选择Ⅱ而不选择Ⅰ的原因是_________________。在反应装置中冷凝水应该从________(填“A”或“B”)端进水。
(3)分离粗产物:反应结束待反应液冷却后,用直形冷凝管换下球形冷凝管,将其变为蒸馏装置进行蒸馏,得到的粗产物中除主产品外,还含下列选项中的________。
①C4H9OH ②SO2 ③(C4H9)2O ④Br2 ⑤NaHSO4⑥H2O ⑦H2SO4
(4)洗涤粗产物:将馏出液移至分液漏斗中,加入等体积的水洗涤后,分液得有机层。如果不能判断哪层是有机层,可以用_______________方法来判断。对有机层,进行洗涤除杂、除水后可得到粗产品。
(5)收集产物:将干燥好的产物移至小蒸馏瓶中,加热蒸馏,收集99~103 ℃的馏分。要证明最终产物是nC4H9Br,方法是_____________________________
___________________________________________。
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。为测定补血剂中铁元素的含量,某化学兴趣小组设计了两套实验方案:
方案一 滴定法 用酸性KMnO4溶液滴定测定铁元素的含量。
反应原理:5Fe2++MnO4—+8H+===5Fe3++Mn2++4H2O
(1)实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需________(填仪器名称)。
(2)上述实验中KMnO4溶液需要酸化,用于酸化的酸是________。
| A.稀硫酸 | B.浓硝酸 | C.稀硝酸 | D.稀盐酸 |
(3)某同学设计的下列滴定方式中,最合理的是________(夹持部分略去)(填字母序号)。
方案二 重量法 操作流程如下:
(4)步骤②中除用H2O2外还可以使用的物质是__________________________。
(5)步骤②是否可以省略________,理由是________________________________
_______________________________________。
(6)步骤④中一系列操作依次是:过滤、洗涤、________、冷却、称量。
(7)假设实验无损耗,则每片补血剂含铁元素的质量________g(用含a的代数式表示)。
硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]为浅绿色晶体,易溶于水,不溶于酒精,在水中的溶解度比FeSO4或(NH4)2SO4都要小。实验室中常以废铁屑为原料来制备,其步骤如下:
图1
步骤1:铁屑的处理。将废铁屑放入热的碳酸钠溶液中浸泡几分钟后,用图1所示方法分离出固体并洗涤、干燥。
步骤2:FeSO4溶液的制备。将处理好的铁屑放入锥形瓶,加入过量的3 mol·
L-1H2SO4溶液,加热至充分反应为止。趁热过滤(如图2所示),收集滤液和洗涤液。
图2
步骤3:硫酸亚铁铵的制备。向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过加热浓缩、冷却结晶、过滤、乙醇洗涤后得到硫酸亚铁铵晶体。
请回答下列问题:
(1)步骤1中图1分离方法称为________法。
(2)步骤2中有一处明显不合理的是___________________________________。
趁热过滤的理由是________________________________________________。
(3)步骤3加热浓缩过程中,当________时停止加热。用无水乙醇洗涤晶体的原因是______________________________________________________________。
(4)FeSO4·7H2O在潮湿的空气中易被氧化成Fe(OH)SO4·3H2O,写出该反应的化学方程式________________________________________________________。
对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂、浓硫酸为催化剂,通过甲苯的硝化反应制备。
一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐(有脱水作用),45 ℃反应1 h。反应结束后,过滤,滤液分别用5% NaHCO3溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
(1)上述实验中过滤的目的是_____________________________________。
(2)滤液在分液漏斗中洗涤静置后,有机层处于________层(填“上”或“下”);放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有_________________________________________________________。
(3)下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
| 催化剂 |
 |
硝化产物中各种异构体质量分数(%) |
总产率(%) |
||
| 对硝基甲苯 |
邻硝基甲苯 |
间硝基甲苯 |
|||
| 浓H2SO4 |
1.0 |
35.6 |
60.2 |
4.2 |
98.0 |
| 1.2 |
36.5 |
59.5 |
4.0 |
99.8 |
|
| NaHSO4 |
0.15 |
44.6 |
55.1 |
0.3 |
98.9 |
| 0.25 |
46.3 |
52.8 |
0.9 |
99.9 |
|
| 0.32 |
47.9 |
51.8 |
0.3 |
99.9 |
|
| 0.36 |
45.2 |
54.2 |
0.6 |
99.9 |
①NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为________。
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是_________________________________________________________。
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有________________、________________。
苯乙醚是一种无色油状液体,熔点-30 ℃,沸点 172 ℃,不溶于水,易溶于醇和醚,广泛用于有机合成中间体及制造医药、染料等。实验合成的原理为:
主要实验步骤如下:
(Ⅰ)合成:在烧瓶中(装置如图)加入7.53 g苯酚、3.92 g NaOH和4 mL水,开动搅拌器,使固体全部溶解,加热反应器控制温度80~90 ℃之间,并用滴液漏斗慢慢滴加8.59 mL溴乙烷(沸点38.4 ℃),大约40 min滴加完毕,继续搅拌1 h,冷却至室温。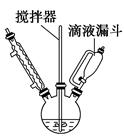
(Ⅱ)分离与提纯。
①加入适量的水(10~15 mL)使固体完全溶解,将液体转入分液漏斗中,分出水相;
②水相用8 mL乙醚萃取一次,与有机相合并;
③有机相用等体积饱和食盐水洗两次,分出水相,再将水相用6 mL乙醚萃取一次,与有机相合并;
④有机相用无水氯化钙干燥;
⑤先用水浴蒸出乙醚,然后常压蒸馏,收集148 ℃稳定的馏分得苯乙醚;
⑥称量产品质量3.69 g。
回答下列问题:
(1)用图示的滴液漏斗代替普通漏斗滴液,其优点是_______________________。
(2)合成时,开动搅拌器的目的是_______________________________。
(3)控制温度80~90 ℃可采用的方法是________________,两次用乙醚萃取的目的是________________________________________________________。
(4)蒸馏时最后温度稳定在148 ℃左右,其原因是_________________
_______________________________________________________。
(5)本次产率为12.4%,产率偏低的原因可能有__________________________
______________________________________________。