由正丁醇(用nC4H9OH表示)制备正溴丁烷(沸点:101.6 ℃)的反应如下:nC4H9OH+NaBr+H2SO4―→nC4H9Br+NaHSO4+H2O
副反应:nC4H9OH CH3CH2CHCH2↑+H2O
CH3CH2CHCH2↑+H2O
2nC4H9OH (nC4H9)2O+H2O
(nC4H9)2O+H2O
3H2SO4(浓)+2NaBr(固)=2NaHSO4+Br2↑+SO2↑+2H2O
已知反应物及其用量:固体NaBr 0.24 mol,nC4H9OH 0.20 mol,浓H2SO4 29 mL,H2O 20 mL。
制备过程经历如下五个步骤,试回答下列问题:
(1)投料:在圆底烧瓶中加入20 mL水,再慢慢加入29 mL浓硫酸,混合均匀并冷却至室温后,再依次加入0.20 mol正丁醇(约18 mL)和0.24 mol溴化钠,充分振荡后加入几粒沸石。
①冷却至室温后再加正丁醇和溴化钠的目的是________。
| A.减少HBr的挥发 |
| B.防止正丁醇的挥发 |
| C.防止溴化钠被氧化 |
| D.防止温度过高导致炭化结焦 |
②本反应中硫酸与溴化钠作用生成氢溴酸,氢溴酸与正丁醇作用发生取代反应生成正溴丁烷。硫酸的用量和浓度过大都对本制备不利的主要原因是
_____________________________________________________。
(2)加热回流:反应装置选择Ⅱ而不选择Ⅰ的原因是_________________。在反应装置中冷凝水应该从________(填“A”或“B”)端进水。
(3)分离粗产物:反应结束待反应液冷却后,用直形冷凝管换下球形冷凝管,将其变为蒸馏装置进行蒸馏,得到的粗产物中除主产品外,还含下列选项中的________。
①C4H9OH ②SO2 ③(C4H9)2O ④Br2 ⑤NaHSO4 ⑥H2O ⑦H2SO4
(4)洗涤粗产物:将馏出液移至分液漏斗中,加入等体积的水洗涤后,分液得有机层。如果不能判断哪层是有机层,可以用_______________方法来判断。对有机层,进行洗涤除杂、除水后可得到粗产品。
(5)收集产物:将干燥好的产物移至小蒸馏瓶中,加热蒸馏,收集99~103 ℃的馏分。要证明最终产物是nC4H9Br,方法是_____________________________
___________________________________________。
实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:
| 实验次数 |
起始温度t1/℃ |
终止温度t2/℃ |
|
| 盐酸 |
NaOH溶液 |
||
| 1 |
20.2 |
20.3 |
23.7 |
| 2 2 |
20.3 |
20.5 |
23.8 |
| 3 |
21.5 |
21.6 |
24.9 |

完成下列问题:
(1)不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是_ 。
(2)在操作正确的前提下,提高中和热测定准确性的关键是_____________。大烧杯如不盖硬纸板,求得的中和热数值将 (填“偏大”、“偏小”或“无影响”)。结合日常生活实际该实验在 中(家用产品)效果更好。
(3)根据上表中所测数据进行计算,则该实验测得的中和热ΔH=___ [盐酸和NaOH溶液的密度按1 g·cm-3计算,反应后混合溶液的比热容(c)按4.18 J·(g·℃)-1计算]。
(4)如用0.5 mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将___ _(填“偏大”、“偏小”、“不变”)。如改用60 mL0.5 mol/L的盐酸与50 mL 0.55 mol·L-1的NaOH 溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”)。
(5)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是 。
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.在量取盐酸时仰视计数
F.大烧杯的盖板中间小孔太大
已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。(提示:碱石灰是生石灰与氢氧化钠的混合物,可以吸收水和二氧化碳)
主要实验步骤如下:① 按图组装仪器,并检验装置的气密性
②将10.0 g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U型管的质量,得到20.0 g
④从分液漏斗滴入6 mol·L-1的硫酸,直到不再产生气体时为止
⑤从导管A处缓缓通入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到22.0 g
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为22.2 g
请填空和回答问题:
(1)装置中干燥管B的作用________________________。如果没有连接该干燥管,测试的结果________________________(填偏高、偏低或不变)。
(2)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果________(填偏高、偏低或不变)。
(3)步骤⑤的目的是________________________,如果没有进行步骤⑤的操作,测试的结果________________(填偏高、偏低或不变)。
(4)试样中纯碱的质量分数为________________________。
实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液500 mL.根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是 (填序号),配制上述溶液还需用到的玻璃仪器是 (填仪器名称).
(2)根据计算用托盘天平称取NaOH的质量为 g.
(3)配制时,其正确的操作顺序是 。(字母表示,每个字母只能用一次)
| A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶 |
| B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解 |
| C.将溶解的氢氧化钠溶液沿玻璃棒注入容量瓶中 |
| D.将容量瓶盖紧,振荡,摇匀 |
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处
(4)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为: mL(计算结果保留一位小数).如果实验室有15 mL、20 mL、50 mL量筒,应选用 mL的量筒最好。
实验室欲配制6.0mol/L的H2SO4溶液,现有三种不同浓度的硫酸:
①480mL 0.5mol/L的硫酸;②150mL 25%的硫酸(ρ=1.18g/mL);③足量的18mol/L的浓硫酸.有三种规格的容量瓶:250mL、500mL、1000mL.配制要求:①②两种硫酸全部用完,不足的部分由③来补充.
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为________mol/L(保留1位小数).
(2)配制时的操作如下,请将操作步骤B、D补充完整.
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18mol/L的浓硫酸________mL,沿玻璃棒缓缓倒入上述混合液中,并不断搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入________mL容量瓶中;
D._________________________________;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1cm~2cm处,改用胶头滴管滴加,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀.
(3)容量瓶使用前需________,瓶上标有________、________、________
(4)进行操作C前还需注意__________________,否则会使所配溶液的浓度_______(填“偏大”、“偏小”或“无影响”).
某实验小组设计用50 mL 1.0 mol/L盐酸跟50 mL 1.1 mol/L氢氧化钠溶液在上图装置中进行中和反应。在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过。通过测定反应过程中所放出的热量可计算中和热。试回答下列问题: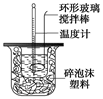
(1)环形玻璃搅拌棒的作用是 。
(2)本实验中用稍过量的NaOH的原因教材中说是为保证盐酸完全被中和。试问:盐酸在反应中若因为有放热现象,而造成少量盐酸在反应中挥发,则测得的中和热____________(填“偏大”“偏小”或“不变”)。
(3)该实验小组做了三次实验,每次取溶液各50 mL,并记录如下原始数据。
| 实验序号 |
起始温度t1/℃ |
终止温度t2/℃ |
温差(t2-t1)/℃ |
||
| 盐酸 |
NaOH溶液 |
平均值 |
|||
| 1 |
25.1 |
24.9 |
25.0 |
31.6 |
6.6 |
| 2 |
25.1 |
25.1 |
25.1 |
30.6 |
5.5 |
| 3 |
25.1 |
25.1 |
25.1 |
31.9 |
6.8 |
已知盐酸、NaOH溶液密度近似为1.00 g/cm3,中和后混合液的比热容C=4.18×10-3 kJ/(g·℃),则该反应的中和热为ΔH=___________________。
(4)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会_______________(填“偏大”“偏小”或“不变”),其原因是___________。
(5)在中和热测定实验中测量起始温度时需要两个温度计,如果只用一个温度计测量,则测得的中和热数值_______________(填“偏大”“偏小”或“不变”)。