在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察右图,然后回答问题。
(1)图中所示反应是_________(填“吸热”或“放热”,1分)反应,该反应________(填“需要”或“不需要”,1分)加热,该反应的△H=____________(用含E1、E2的代数式表示,1分)。
(2)已知热化学方程式:H2(g)+1/2O2(g)=H2O(g);△H=-241.5 kJ/mol,该反应的活化能为167.4 kJ/mol,则其逆反应的活化能为_________________。
(3)对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是_____________________。
(10分)在密闭容器里,通入x mol H2(g)和y molI2(g),发生反应
H2(g)+I2(g) 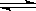 2HI(g)△H<0。改变下列条件,反应速率将如何改变?(填“增大”“减小”或“不变”)
2HI(g)△H<0。改变下列条件,反应速率将如何改变?(填“增大”“减小”或“不变”)
(1)升高温度;(2)扩大容器的体积;
(3)充入更多的H2;(4)容器容积不变,通入氖气;
(1)Zn∣H2SO4溶液∣C原电池:负极反应
正极反应;电池反应
(2)H2∣KOH溶液∣O2原电池:负极反应
正极反应;电池反应
在101kPa时,0.5molCH4完全燃烧生成CO2和液态H2O放出495.2kJ的热量,写出该反应的热化学方程式。.
100mL浓度为2mol•L-1的硫酸与过量锌粒反应,为加快反应速率,又不影响生成氢气的总量,可采取的方法是。
| A.加入适量的6mol•L-1的硫酸 | B.将锌粒改为锌粉 | C.加入适量的KCl溶液 | D.升高溶液温度E.加入适量硫酸铜 |
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示: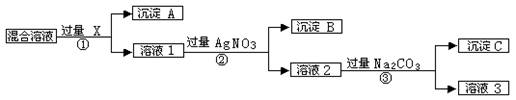
请回答下列问题:
⑴写出实验流程中下列物质的化学式:试剂X:,沉淀A:,沉淀B:。
⑵上述实验流程中加入过量的Na2CO3的目的是。
⑶按此实验方案得到的溶液3中肯定含有杂质(填化学式);为了解决这个问题,可以向溶液3中加入适量的,之后若要获得固体NaNO3需进行的实验操作是(填操作名称)。