下列反应既属于氧化还原反应,又是吸热反应的是( )
| A.铝和盐酸反应 | B.灼热的木炭与CO2反应 |
| C.氢气还原氧化铜 | D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应 |
25℃时,某溶液中由水电离产生的c(H+)和c(OH-)的乘积为1×10-18,下列说法正确的是
| A.该溶液的pH可能是5 | B.此溶液不存在 |
| C.该溶液的pH一定是9 | D.该溶液可能pH=7 |
在密闭容器中,对于可逆反应A +3B  2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
| A.若正反应方向△H <0,则T1> T 2 |
| B.压强增大时,混合气体的平均相对分子质量减小 |
| C.A一定为气体 |
| D.B一定为气体 |
下列溶液中有关物质的浓度关系正确的是
| A.c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液:c(NH4HSO4) > c[ (NH4)2SO4]> c(NH4Cl) |
| B.等物质的量的NaClO、NaHCO3混合溶液: c(HClO)+c(ClO-) = c(HCO3-) + c(H2CO3) + c(CO32-) |
| C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液: c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) |
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系;当在某一温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二。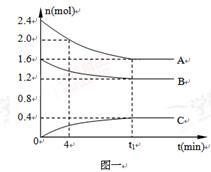
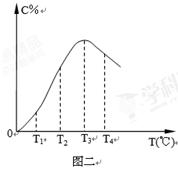
下列分析不正确的是:
A.0~4分钟时,A的平均反应速率为0.02mol/(L•min)
B.该反应的平衡常数表达式K=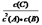
C.由T1向T2变化时,正反应速率大于逆反应速率
D.此反应的正反应为放热反应
X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素在地壳中的含量最多,Z元素的化合物的焰色反应呈黄色,R原子的核外电子数是X原子与Z原子的核外电子数之和。下列叙述不正确的是
| A.X与Y能形成两种常见的气态化合物 |
| B.原子半径的大小顺序:r(Z)>r(R)> r(X)>r(Y) |
| C.X、Z分别与R形成的化合物中化学键类型不同 |
| D.含有Y、Z、R三种元素的化合物最多只有2种 |