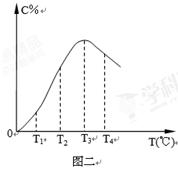
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系;当在某一温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二。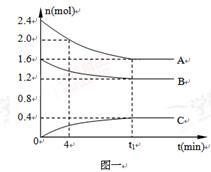
下列分析不正确的是:
A.0~4分钟时,A的平均反应速率为0.02mol/(L•min)
B.该反应的平衡常数表达式K=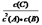
C.由T1向T2变化时,正反应速率大于逆反应速率
D.此反应的正反应为放热反应
下列有关物质性质的比较顺序中,不正确的是
| A.热稳定性:HF<HCl<HBr<HI | B.微粒半径:K+>Na+>Mg2+>Al3+ |
| C.酸性:HClO4>H2SO4>H3PO4>H2SiO3 | D.熔点:Li>Na>K>Rb |
2001年诺贝尔化学奖授予“手性碳原子的催化氢化、氧化反应”研究领域作出贡献的美、日三位科学家。在有机物分子中,当碳原子连有4个不同的原子或原子团时,这种碳原子称为“手性碳原子”,凡具有一个手性碳原子的化合物一定具有光学活性。下列分子中含有“手性碳原子”的是
| A.CBr2F2 | B.CH3CH2OH |
| C.CH3CH2CH3 | D.CH3CH(OH)COOH |
氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如下图所示。常温下S2Cl2是一种橙 黄色的液体,遇水剧烈反应,并产生能使品红褪色的气体。下列说法错误的是
黄色的液体,遇水剧烈反应,并产生能使品红褪色的气体。下列说法错误的是
| A.S2Cl2的结构式为Cl—S—S—Cl |
| B.S2Cl2为含有极性键和非极性键的非极性分子 |
| C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2 |
| D.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2 + 2H2O = SO2↑ + 3S↓ + 4HCl |
用价层电子对互斥理论(VSEPR模型)预测H2S和COCl2的立体结构,两个结论都正确的是
| A.直线形;三角锥形 | B.V形;三角锥形 |
| C.直线形;平面三角形 | D.V形;平面三角形 |
已知某+2价离子的电子排布式为1s22s22p63s23p63d9,该元素在周期表中所属的族是
| A.ⅠB | B.ⅡB | C.Ⅷ | D.ⅡA |