乙醇分子中不同的化学键如下,关于醇在各种不同反应中断裂的键说明不正确的是( )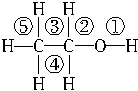
| A.和金属钠反应时键①断裂 |
| B.和浓H2SO4共热到170 ℃时断键②和⑤ |
| C.在银催化条件下与O2反应时断键①和③ |
| D.和浓H2SO4共热到140 ℃时断键②,其他键不变化 |
已知铍(Be)的原子序数为4,下列对铍及其化合物的叙述中,正确的是 ( )
| A.铍的原子半径大于硼的原子半径 |
| B.氯化铍分子中铍原子的最外层电子数是8 |
| C.氢氧化铍的碱性比氢氧化钙的弱 |
| D.单质铍跟冷水反应产生氢气 |
下列叙述正确的是 ()
| A.同主族金属的原子半径越大熔点越高 |
| B.稀有气体原子序数越大沸点越高 |
| C.分子间作用力越弱分子晶体的熔点越低 |
| D.同周期元素的原子半径越小越易失去电子 |
下列说法正确的是 ()
()
| A.原子半径:Cl>S>P | B.还原性:Na>Mg>Al |
| C.稳定性:HF>HCl>HBr | D.酸性:HClO4>H2SO4>H3PO4 |
下列各组化合物中的氮元素,具有相同化合价的是()
| A.NO和NO2 | B.NO2和N2O4 | C.NH3和NH4Cl | D.N2O和HNO2 |
下列物质能使无色酚酞试液变红的是()
| A.苛性钠 | B.纯碱 | C.熟石灰 | D.食盐 |