实验室常用下列装置来制取氧气:
(1)写出图中有标号仪器的名称:a 、b ;
(2)用过氧化氢溶液和二氧化锰来制取氧气时,可选用的发生装置是 (填序号);
(3)用E装置收集氧气的依据是
检验氧气是否集满的方法是
(4)写出一个实验室制取氧气的文字表达式为
该反应属于哪种基本反应类型 ;
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下氨气是一种无色、有刺激性气味的气体,密度比空气小。氨气极易溶于水。制取并收集氨气,应该从上图中选择的发生装置是 ,收集装置是______;
(6)一氧化氮气体密度比空气大,常温下会与氧气反应生成二氧化氮,一氧化氮气体不易溶于水。则收集一氧化氮气体的装置是
(7)在医院里给病人输氧时,在氧气钢瓶和病人吸氧器之间连接一个类似右图所示的装置,在装置中盛放大约半瓶蒸馏水,导气管 (填“a”或“b”)端连接在供氧气的钢瓶上。
为了探究二氧化碳能否与水发生反应生成具有酸性的物质,A、B两同学分别设计了探究实验的方案。A同学的实验方案是将二氧化碳通入紫色石蕊试液中,观察溶液的颜色变化,如图甲所示。B同学的实验方案是取四朵用石蕊试液染成紫色的干燥的小花,按图乙进行实验,观察小花颜色变化(紫色石蕊试液遇酸变红色)。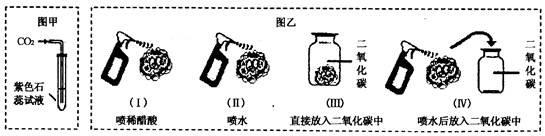
(1)图乙中,观察到纸花的颜色变化是:I.纸花变红 Ⅱ.Ⅲ.纸花不变色 Ⅳ.
写出实验Ⅳ中发生反应的文字表达式: 。
(2)哪个同学的方案合理。
(3)该方案合理的理由是。
已知某合金粉末除铝外,还含有铁、铜中的一种或两种。某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究。
【查阅资料】铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应。
【猜想】猜想1:该合金粉末中除铝外,还含有铁。
猜想2:该合金粉末中除铝外,还含有(填名称)。
猜想3:该合金粉末中除铝外,还含有铁、铜。
【实验探究】下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液。
| 实验方案 |
实现现象 |
结论 |
| ①取一定量的合金粉末,加过量的 ,充分反应后过滤,滤渣备用。 |
粉末部分溶解,并有气体放出。 |
合金中一定含有。 |
| ②取步骤①所得滤渣,加过量的 ,充分反应。 |
滤渣部分溶解,并有气体放出,溶液呈浅绿色。 |
合金中一定含有。 |
【探究结论】猜想3成立。
【反思】一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质。写出铝与稀盐酸反应的化学方程式。
在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整。
【实验目的】铁生锈条件的探究。
【实验内容】取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象。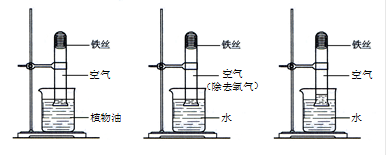
【实验现象】实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小。
【实验结论】铁生锈实际上是铁与空气中的(填名称)发生反应的结果。
【实验思考】
(1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的。
(2)该实验创新之处在于:可根据铁丝表面的铁锈和两种现象来判断铁丝反应进行的情况。
(3)用完的菜刀要擦干存放,理由是。
(4)铝比铁活泼,但铝难腐蚀,原因是。
2009年2月12日,我外交部就法国某公司拍卖我国两件重要文物兔首和鼠首(见右图),发表严正声明:中国对其拥有不可置疑的所有权。目前我国正在积极追讨这两件文物。兔首和鼠首均为青铜器(铜、锡合金),表面呈绿色,这是铜器长期暴露在空气中生成了铜锈(铜锈俗称铜绿)。为了弄清铜绿的组成和铜生成铜绿的条件,某化学实验小组进行了如下探究:
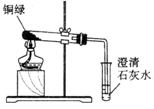
1.探究铜绿的组成
【查阅资料】通过查阅资料知道:铜绿受热易分解。
【设计与实验】
(1)小芳从其它铜器上取下适量的干燥铜绿,按右图所示装置进行实验。在实验过程中,观察到:试管口内有水珠出现,说明了铜绿中含有氢、氧元素;澄清石灰水变浑浊,说明了铜绿中含有元素。
(2)小芳取下少量试管内反应后的剩余物,放入另一支试管中,滴人稀硫酸,充分反应后,溶液变蓝色,说明铜绿中含有元素。
【实验结论】铜绿是由铜、氢、氧和碳元素组成的。
2.探究铜生成铜绿的条件
【查阅资料】铜绿的化学式是Cu2(OH)2CO3,它受热会分解生成三种氧化物。铜绿分解的化学方程式为。
【猜想与假设】据铜绿的组成和查阅的资料判断,铜绿可能是铜与氧气及共同作用而形成的。
【设计与实验】借鉴课本“铁钉锈蚀条件的探究”实验,小梁设计了“铜片锈蚀条件的探究”实验,实验如下图所示(所用铜片洁净、光亮,试管内的“”为铜片):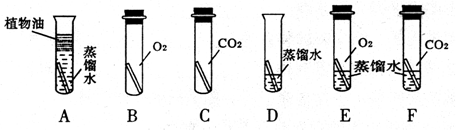
实验较长时间后,发现试管中铜片最先生锈(填试管字母编号)。
【评价与改进】小区认为小梁设计的实验还不够完善,要得出正确的结论,还要补充一个实验。你认为要补充的一个实验是(用图表示亦可)。
【拓展与应用】
小明发现从不同地点收集到的两个铜器(一个是纯铜做的,一个是青铜做的)中,纯铜器的铜绿比青铜器的少,他据此分析认为青铜比纯铜易锈蚀。小明的分析是否全面?请你说明理由。
。
铜器长期暴露在空气中会生成铜绿(俗称铜锈)。铜锈的主要成分是碱式碳酸铜,碱式碳酸铜不稳定,受热分解成黑色固体物质、无色气体和水。这种黑色固体和无色液体的成分是什么呢?
查阅资料:碱式碳酸铜的化学式是Cu2(OH)2CO3。稀硫酸能与Fe2O3、CuO等金属氧化物反应,生成盐和水。
提出猜想:某同学根据碱式碳酸铜的化学式对黑色固体、无色液体的成分做出了一下猜想:
①无色气体为二氧化碳;②黑色固体为氧化铜;③…
实验验证:实验装置如图。
在此实验装置中,大试管的管口略向下倾斜的目的是。
验证①:若猜想①正确,实验过程中应该看到澄清的石灰水。 产生此现象的化学方程式是。在反应完全停止加热时,针对熄灭酒精灯和把导管移出液面这两步操作,你认为应该先进行的操作是。
验证②:从装置中取下大试管并冷却到室温,然后向大试管中加入足量的稀硫酸,充分振荡,静置后观察实验现象。若猜想②正确,观察到得实验现象应该是,发生反应的化学方程式为。