根据下表回答问题。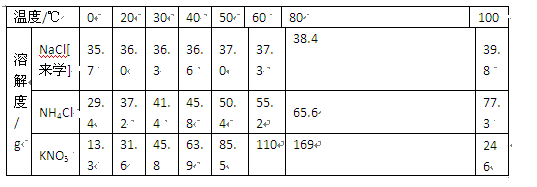
(1)硝酸钾溶液中的溶质为 。
(2)20℃时,向100 g水中加入36 g氯化铵,充分溶解后得到 (填“饱和”或“不饱和”)溶液。
(3)20℃时,向100 g水中加入50 g氯化钠,若使氯化钠完全溶解,可以采用的方法是 。
(4)有一杯80℃的KNO3不饱和溶液(如图A,水为100 g),经过如下图的变化过程(在整个过程中水分的蒸发忽略不计)。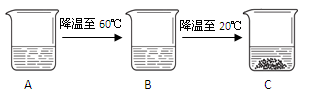
① C烧杯溶液中溶质的质量为 g。
② 有关三个烧杯中溶液的下列说法中,不正确的是 (填字母序号)。
a.B烧杯中的溶液一定是不饱和溶液
b.在变化过程中,溶解度一定发生改变
c.由60℃降温至50℃时溶液质量有可能减少
d.A到B的变化过程中,溶液中溶质质量没有发生改变
甲、乙两种物质的溶解度曲线如图.
(1)10℃时,甲物质的溶解度 (选填“大于”、“小于”或“等于”)乙物质的溶解度.
(2)40℃时,把40g甲物质放入100g水中,所得的是 (选填“饱和”或“不饱和”)溶液.
(3)20℃时,甲物质溶液中溶质的质量分数不可能为 .
A.20%B.25%C.26.5%D.30%

在一个密闭容器中有A、B、C、D四种物质,在一定条件下充分反应,测得数据如表:
|
物质 |
A |
B |
C |
D |
|
反应前的质量/g |
6.4 |
3.2 |
4.0 |
2.8 |
|
反应后的质量/g |
5.2 |
待测 |
7.2 |
2.0 |
反应后待测的B的质量是 克,该反应所属的基本反应类型是 。
根据如图标签上的信息填空.
(1)写出物质中阴离子的符号 .
(2)标出硝酸钠中氮元素的化合价 .

赣南的客家围屋如同城堡,可以抵御外敌入侵。现有五种物质盐酸、硫酸、氢氧化钠、氯化钡和碳酸钠作为围屋的守护“卫士”,只有相邻物质间能发生反应才能组成守护的防线(如图所示)。其中物质A常用于铅酸蓄电池中,其浓溶液有脱水性;物质C是人体胃液中的主要成分。(提示:碳酸钡不溶于水)
(1)A物质是 。
(2)B与C反应的化学方程式为 ;A与E反应时的实验现象为 。
(3)现有下列物质作为“外敌”分别对围屋发起进攻,若该物质与两位相邻的守护“卫士”都能发生反应才能攻破防线,那么能攻入围屋的物质是 (填序号)。
①铁 ②氧化铁 ③二氧化碳 ④氢氧化钡。

高锰酸钾是常用的氧化剂。如图是实验室模拟工业上制备高锰酸钾晶体的操作流程:

(1)完成操作③所需要的玻璃仪器是 (填一种即可);实验中通过操作②所析出高锰酸钾晶体,说明高锰酸钾的溶解度随温度升高而 ;
(2)操作流程中可循环利用的物质是 ;
(3)氢氧化钾、二氧化锰和氧气在高温条件下煅烧,生成锰酸钾和水,该反应的化学方程式为 。