下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A.0.1mol·L-1NH4Cl溶液:c(NH4+)=c(Cl-) |
| B.0.1mol·L-1 Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液: c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) |
限用硝酸、硫酸、盐酸、醋酸、钠盐、钾盐、钡盐等两两相互反应,并符合离子方程式:
2H++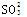 = H2O+SO2↑的化学反应个数有
= H2O+SO2↑的化学反应个数有
| A.4 | B.5 | C.8 | D.12 |
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.500 mL 2 mol·L-1 FeCl3溶液中Fe3+数为NA,且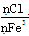 =3 =3 |
| B.1 L pH=1的硫酸溶液中含有的H+为0.2NA |
| C.标准状况下,22.4L 乙烷中含极性共价键的数目为7NA |
| D.12 g石墨和C60的混合物中质子总数一定为6NA个 |
某可逆反应aA + bB cC ;ΔH= -QkJ/mol;在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为
cC ;ΔH= -QkJ/mol;在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为
A.写成2aA + 2bB 2cC,Q值、K值均扩大了一倍 2cC,Q值、K值均扩大了一倍 |
B.写成2aA + 2bB 2cC,Q值扩大了一倍,K值保持不变 2cC,Q值扩大了一倍,K值保持不变 |
C.写成cC aA + bB,Q值、K值变为原来的相反数 aA + bB,Q值、K值变为原来的相反数 |
D.写成cC aA + bB,Q值变为原来的相反数,K值变为倒数 aA + bB,Q值变为原来的相反数,K值变为倒数 |
假设SiO2原子晶体中Si原子被Al原子取代,不足的价数由K原子补充。当有25%的硅原子被铝原子取代时,可形成正长石,则正长石的化学组成为
A.KAlSiO4B.KAlSi2O6D.KAlSi3O8D.KAlSi4O10
下列物质中既能跟稀H2SO4反应, 又能跟氢氧化钠溶液反应的是
①NaHCO3②Al2O3③Al(OH)3④(NH4)2S
| A.③④ | B.②③④ | C.①③④ | D.全部 |