H、D、T三种微粒,它们相互之间关系是 ,
同温同压下,它们单质的密度之比是 ,
在1mol单质中,它们的质子数之比是 ,
在相同状况下,1L单质中,它们的电子数之比是 。
在工农业生产和日常生活中经常用到下列物质:
①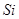 ;②
;②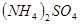 ;③
;③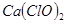 ;④
;④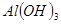 ;⑤
;⑤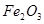 。其中,可用于制造芯片的是__________(填序号,下同);可用于杀菌,消毒的是__________;可用作化肥的是__________;可用作红色油漆和涂料的是______________;医疗上可用作胃酸中和剂的是_______。
。其中,可用于制造芯片的是__________(填序号,下同);可用于杀菌,消毒的是__________;可用作化肥的是__________;可用作红色油漆和涂料的是______________;医疗上可用作胃酸中和剂的是_______。
某同学欲探究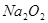 与水的反应,可供使用的试剂有:
与水的反应,可供使用的试剂有: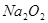 、蒸馏水、
、蒸馏水、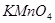 酸性溶液、
酸性溶液、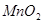 。该同学取一定量
。该同学取一定量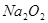 样品与过量水反应,待完全反应后,得到溶液X和一定量氧气
样品与过量水反应,待完全反应后,得到溶液X和一定量氧气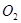 ,该同学推测反应中可能生成了
,该同学推测反应中可能生成了 ,并进行实验探究。
,并进行实验探究。
(1)试设计实验证明溶液X中含过氧化氢____________________________。
(2)通过上述实验证明溶液中确实存在 ,取少量X于试管中,滴加几滴酚酞试液,实验现象为___________________________________。
,取少量X于试管中,滴加几滴酚酞试液,实验现象为___________________________________。
(3)取少量X于试管中,滴加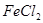 溶液,立即生成红褐色沉淀,则该反应的离子方程式为____________________________。
溶液,立即生成红褐色沉淀,则该反应的离子方程式为____________________________。
(4)已知溶液X可使酸性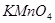 溶液褪色,同时放出氧气,完成并配平该反应的离子方程式:_______
溶液褪色,同时放出氧气,完成并配平该反应的离子方程式:_______ _______
_______ +_______
+_______ -_______
-_______ +_______
+_______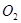
 +
+
_______ 。
。
铝土矿的主要成分是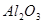 ,含有杂质
,含有杂质 、
、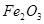 、
、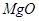 。工业上从铝土矿中提取铝可采用如下工艺流程:
。工业上从铝土矿中提取铝可采用如下工艺流程:
请回答下列问题:
(1)图中涉及分离溶液与沉淀的实验方法是____________(填操作名称)。
(2)沉淀B的成分是____________(填化学式,下同),B可以用来制作普通玻璃,化学方程式是____________________,____________________;沉淀C的成分是____________;溶液D中存在较多的阴离子是____________。
(3)沉淀F转化为物质M的化学方程式为________________________;由物质M制取铝的化学方程式为________________________;溶液D中通入过量 生成沉淀F的离子方程式为________________________。
生成沉淀F的离子方程式为________________________。
工业上用电解饱和食盐水的方法生产氯气和烧碱。
(1)食盐溶于水发生电离,其电离方程式为____________________________________。
(2)2004年4月15日,某化工厂发生氯气泄漏事件,工作人员喷射 溶液形成液幕,包围并吸收泄漏的氯气,其反应原理为__________________(用离子方程式表示)。
溶液形成液幕,包围并吸收泄漏的氯气,其反应原理为__________________(用离子方程式表示)。
(3)事件过后,附近居民向记者反映当时晾在外面的衣服褪色了,其原因是_________
___________________________(结合化学方程式解释)。
碳酸钠和碳酸氢钠是生活中常见的物质。请回答下列问题。
(1)碳酸氢钠的化学式是_________,俗称_________,其水溶液显_________性(填“酸”、“碱”或“中”)。
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为_________。等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成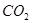 的量,前者_________后者(填“>”、“<”或“=”)
的量,前者_________后者(填“>”、“<”或“=”)
(3)除去碳酸钠固体中碳酸氢钠的反应的化学方程式为__________________________。