在古代,人们常用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和纯碱为原料制取烧碱,某小组同学按图所示流程进行实验,请你参与讨论并回答相关问题.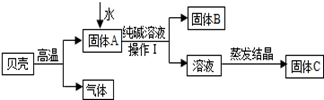
Ⅰ.定性研究
(1)生成固体B的化学反应方程式______________________________________________;
(2)操作Ⅰ指的是______________,其中要用到的玻璃仪器有烧杯、玻璃棒、 ;
(3)溶液蒸发结晶得到固体C的过程中,常用玻璃棒搅拌,其目的是__________________。
【猜想与假设】小组同学根据实验流程对所得的固体C的组成提出了质疑:甲同学认为:可能是NaOH、Na2CO3;乙同学认为: 可能是 ; 丙同学认为:可能是NaOH
【交流与评价】请你把乙同学的可能猜想结果写在横线上;
【活动与探究】甲同学取原溶液向其中倾倒一定量的稀盐酸观察到有大量气泡产生,于是得出该溶液中的溶质是NaOH、Na2CO3的结论,证实了自己的猜想。
乙同学取原溶液向其中加入Na2CO3溶液无现象,据此否定了自己的猜想;他又重新取原溶液,向其中加入____________观察到与甲同学不同的现象,得出了和甲同学相同的结论。
丙同学为了验证上述结论也取原溶液向其中滴加了少量稀盐酸,却发现无气泡产生。
【解释与结论】大家经过分析找出了丙同学所用试剂与甲同学相同,却没有看到气泡的原因。你认为可能的原因是 。经过上述三位同学的共同努力,大家终于对溶液中溶质的成分得出了正确结论。
Ⅱ.定量探究
【提出问题】固体产品C氢氧化钠的质量分数是多少呢?
【设计实验】小组同学设计了两套不同的方案进行实验并测得数据如下: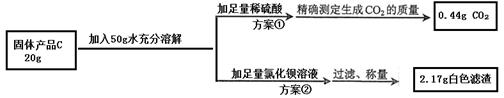
请你利用方案①所得数据计算固体产品C中氢氧化钠的质量分数(请列出计算过程)
【实验反思】
另一组同学根据方案②所得数据计算出的氢氧化钠质量分数与方案①相比明显偏小,请你分析其中的可能原因:_________________________________。
CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质: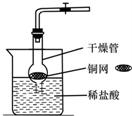
(1)该兴趣小组用干燥管、烧杯、铜网等设计装配了一个在实验室中制取二氧化碳气体的装置,如左图所示.在干燥管内的铜网上应盛放
(2)该兴趣小组同学将制得的CO2分别通人澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象.写出石灰水变浑浊的化学方程式:
CO2和NaOH是否发生了化学反应?
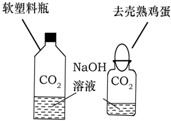
①小明设计了甲、乙两个实验来验证C02与NaOH发生了化学反应,如右图所示.实验现象为:甲--软塑料瓶变瘪,乙--“瓶吞鸡蛋”.小雯同学提出质疑,她认为上述实验还不足以说明CO2和NaOH发生了反应.其理由是
②小虎向甲实验后变瘪塑料瓶的溶液中加入,观察到现象,从而证明CO2与NaOH已经发生了反应.
写出塑料瓶中先后发生的两个化学方程式..
某校化学研究小组对某铜器表面的绿色铜锈展开探究,请回答有关问题。
【实验过程】
(1)动手实验
实验一:
| 实验步骤 |
实验现象 |
实验结论 |
| a.取少量铜锈于试管中,加入适量稀硫酸 |
固体溶解,产生气泡,溶液呈蓝色 |
铜锈溶解后形成的溶液中含有的阳离子是※(写化学符号) |
| b.将生成气体通入澄清石灰水 |
铜锈中含有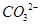 |
实验二:另取少量铜锈隔绝空气加热,发现绿色粉末变黑色,试管壁上有水珠。
【实验结论】综合以上两个实验,可以确认铜锈中含有种元素。
(2)探究铜生锈的条件
【猜想】同学们对空气中有哪些物质参与了铜的生锈作出以下三种猜想:
①CO2、H2O ②O2、H2O ③CO2、H2O、O2
根据铜锈组成元素并结合铁生锈的知识,你认为上述猜想错误的是(填序号)。
【实验设计】为验证另外两种猜想,同学们设计了下图中A、B两个对比实验,请你在方框内完成实验B的设计(语言叙述或画图说明均可)。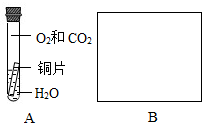
【预计结论】若A中的铜生锈,B中的铜不生锈,则正确的猜想是(填序号)。
近期我市三江县茶叶又在全国评比中获得金奖,可宇弘同学发现他家里承包种植的茶树叶子枯黄和脱落。于是他对此现象进行了资料查阅:他家的茶树适合在偏碱性的土壤中生长,不适合在偏酸性的土壤中生长。
(1)对此他提出以下猜想:①茶树叶子枯黄和脱落,可能是缺少氮肥引起的;②茶树叶子枯黄和脱落,也有可能是土壤呈性引起的。
(2)请你为宇弘同学设计实验来验证土壤的酸碱性,以此证明猜想(2)成立(要求写出实验的步骤、现象和结论。)
(3)通过实验证明了宇弘同学的猜想②是造成茶树叶子枯黄和脱落的原因之一。要改良此土壤,以便适合茶树的生长,你建议宇弘同学应采取的措施是什么?并说出你的理由。
在金属活动性顺序里,钠位于铜之前。某化学兴趣小组发现,将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,却未置换出红色的铜。该小组同学对此现象进行了如下探究:
【查阅资料】钠的化学性质非常活泼,常温下就能被空气中的氧气氧化,且能与水迅速反应。
【分析与讨论】
(1)在实验室中通常将钠保存在煤油里,煤油的作用是。
(2)已知:在一个化学反应中,如果有元素化合价的升高,同时就有元素化合价降低。对于钠与水反应的生成物,甲同学猜想是NaOH和H2,乙同学猜想是NaOH和O2,你认为同学的猜想不合理,请从化合价的角度解释原因:。
【进行实验】该小组同学通过实验验证钠与水反应的产物,装置如下图: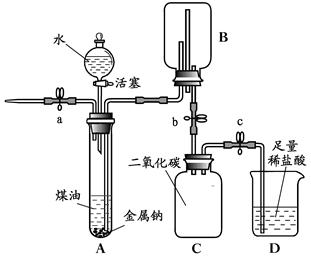
注:煤油的密度为0.8g/mL,与水不互溶。
| 实验操作 |
实验现象及分析 |
|
| ① |
打开止水夹a及分液漏斗活塞,待液体充满大试管后,关闭止水夹a及分液漏斗活塞。 |
实验现象为:液体分层,钠熔成银白色小球,在液体分层的界面上跳动,产生大量气泡,下层液体逐渐被压入B中。 钠的物理性质有:(任写两条)。 |
| ② |
打开止水夹b,待B中部分液体进入C中,迅速关闭止水夹b。 |
发生反应的化学方程式为: 。 |
| ③ |
打开止水夹c。 |
实验现象为:D中液体,C中产生气泡。 |
| ④ |
打开止水夹a,通过分液漏斗向大试管中逐滴加水,将燃着的木条伸至装置左端尖嘴导管口。 |
实验现象为:气体燃烧,产生色火焰。 |
| ⑤ |
在火焰上方罩一个干冷的烧杯。 |
实验现象为:烧杯内壁出现。 |
【解释与结论】将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,写出发生反应的化学方程式(分两步写):,。
根据下列装置图,回答有关问题:
(1)写出装置中标号仪器的名称:a,b。
(2)实验室制取氧气时选用A作为发生装置,若试管中是混有二氧化锰的氯酸钾,该反应的化学方程式为;若试管中是高锰酸钾,则需要在试管口放一团棉花,其目的是。
(3)实验室制取二氧化碳时选用B作为发生装置,该反应的化学方程式为;选用C作为收集装置,则检验二氧化碳是否已收集满的方法是。
(4)实验室用锌粒与稀硫酸反应制取氢气,发生装置如右图所示。打开止水夹,若发现稀硫酸未能与有孔塑料板上的锌粒接触,但此时已无稀硫酸可加,则下列溶液中,最适宜从长颈漏斗中添加的是(选填字母)。
| A.氢氧化钠溶液 | B.碳酸钠溶液 |
| C.硫酸钠溶液 | D.澄清石灰水 |