现有含NH4+、H+、Al3+、Mg2+、Cl-的溶液100mL,往其中逐滴加入2mol/L的氢氧化钠溶液,并不断搅拌,所得沉淀质量与所加氢氧化钠溶液体积的关系如下图,其中OA段无气体产生,回答下列问题。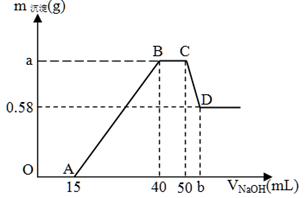
(1)写出下列过程发生反应的离子方程式。
OA段: ;
CD段: ;
(2)氢氧化镁沉淀的质量m[Mg(OH)2] = g。
(3)a = ;b = 。
(4)原溶液中c(NH4+) = ;c(Cl-) = 。
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖。在有机物分子中,不同氢原子的核磁共振谱中给出的吸收峰也不同,根据吸收峰可以确定有机物分子中氢原子的种类和数目。例如二乙醚的结构简式为: CH3—CH2—O—CH2—C H3其核磁共振谱中给出的吸收峰有两个,如图1所示:
H3其核磁共振谱中给出的吸收峰有两个,如图1所示:

(1)下列物质中其核磁共振氢谱中给出的只有一个吸收峰的是。
| A.CH3CH3 | B.CH3COOH | C. CH3COOCH3 | D. CH3OCH3 |
(2)化合物A和B的分子式都是C2H4Br2, A的核磁共振氢谱图如图2所示,
则A的结构简式为:,请预测B的核磁共振氢谱上有个吸收峰。
写出下列反应的化学方程式。
(1)丙醛与银氨溶液水浴加热
(2)用甲苯制TNT的反应
(3)1-溴丙烷与NaOH的乙醇溶液共热
(4)甲酸和2-丙醇在浓硫酸作用下
(1)用系统命名法给 (CH3CH2)2C(CH3)2命名;
(2)1,3-丁二烯的键线式;
(3)羟基的电子式是;
(4) CH2=CH—CHO所含官能团的名称是;该有机物发生加聚反应后,所得产物的结构简式为。
简要回答下列问题。
(1)居室装修完毕,通常要开窗通风一段时间后才能入住,其原因是。
(2)可以用铁罐盛装浓硫酸或浓硝酸的原因是。
(3)医疗上,胃舒平[主要成分Al(OH)3]常用作治疗胃酸(含盐酸)过多的药剂,其理由是。
下表是某地区市场上销售的一种“加碘食盐”包装袋上的部分文字说明。请根据此表,结合初中化学和生物学科的知识,回答下列问题。
| 配料表 |
精制海盐、碘酸钾[ |
| 含碘量 |
20~40mg/kg |
| 卫生许可证号 |
××卫碘字(1999)第001号 |
| 分装日期 |
见封底 |
| 储藏方法 |
密封、避光、防潮 |
| 食用方法 |
烹调时,待食品熟后加入碘盐 |
(1)碘是合成下列哪种激素的主要原料之一()
A.胰岛素 B.甲状腺素 C.生长激素 D.雄性激素
(2)长期生活在缺碘山区,又得不到食盐供应,易患()
A.甲状腺亢进 B.贫血症 C.地方性甲状腺肿大 D.糖尿病
D.糖尿病
(3)食盐中加碘,这碘指的是(填元素、原子或单质)。
(4)碘酸钾的化学式为KIO3,其中碘元素的化合价为____________。
(5)根据含碘盐的食用方法可推测碘元素的化学性质,碘酸钾在受热时容易__________。
(6)已知可用盐酸酸化的碘化钾淀粉溶液,检查食盐中含碘酸钾(进行如下反应:IO3-+5I-+6H+==3I2+3H2O)。现有①纯净水、②白酒、③食醋、④淀粉KI试纸、⑤纯碱,试从中选择必须的物质检验食盐样品中是否加入碘,选择的物质_______________(填序号)。