下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其它为化合物,其中C为两性氧化物。试推断:
(友情提示:金属Al可在高温下将一些金属从其氧化物中置换出来)
(1)写出物质的化学式:
A: B: C: H:
(2)写出下列反应的方程式:
A→D反应的化学方程式
C→F反应的离子方程式
D→G反应的离子方程式
【化学——选修5有机化学基础】
芳香族化合物A,分子式为C9H9OCl,且能发生银镜反应;D为含有八元环的芳香族化合物。A与其它物质之间的转化如下图所示: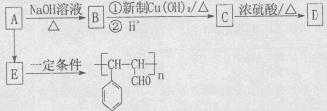
(1)A的结构简式为。
(2)A→E的反应条件为;C→D的反应类型为。
(3)写出B→C第①步的反应方程式。
(4)B的一种同系物F(分子式为C8H8O2)有多种同分异构体,则含有 的芳香族化合物的同分异构体有____种,写出其中核磁共振氢谱有4个峰的一种结构简式。
的芳香族化合物的同分异构体有____种,写出其中核磁共振氢谱有4个峰的一种结构简式。
(5)已知: 由甲苯及其它必要物质经如下步骤也可合成B:
由甲苯及其它必要物质经如下步骤也可合成B:
反应I的试剂及条件为:反应IV所用物质的名称为;
反应III的化学方程式为。
铝是用途广泛的金属材料,目前工业上主要用铝土矿(主要成分含氧化铝、氧化铁)来制取铝,其常见的过程如下: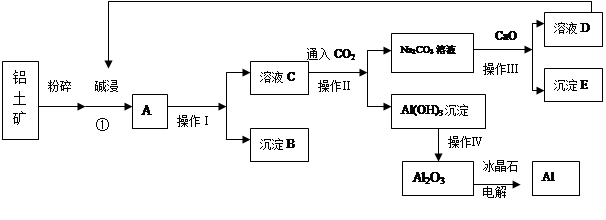
请回答下列问题:
(1)沉淀B的化学式为,溶液C中阴离子主要是。
(2)操作Ⅰ是(填操作名称)
(3)写出①过程中发生反应的离子方程式。
(4)Al(OH)3沉淀必须进行洗涤才能通过操作Ⅳ获得纯净Al2O3,操作Ⅳ是(填操作名称),简述洗涤沉淀的操作方法:。
(5)生产过程中,除水、CaO和CO2可以循环使用外,还可循环使用的物质有(填化学式)。
(6)电解Al2O3制取金属Al的阳极电极反应式为。
乙酰水杨酸俗称阿司匹林,是一种历史悠久的解热镇痛热。合成原理是:
(1)水杨酸中含氧官能团的名称是,有关水杨酸的说法,正确的是。
| A.遇 FeCl3溶液可能显紫色 |
| B.可发生酯化反应和水解反应 |
| C.能与溴水发生取代反应和加成反应 |
| D.1mol水杨酸最多能与3molH2发生加成反应 |
(2)水杨酸与乙酸酐反应的反应类型是。
(3)乙酰水杨酸的分子式为,1mol乙酰水杨酸最多能与molNaOH反应。
(4)虚框中为提纯,是为了除去该反应的副产物:水杨酸、乙酰水杨酸水杨酯、乙酰水杨酸酐和聚合物等请写出乙酰水杨酸粗品中加入饱和Na2CO3溶液发生的主要化学反应方程式为: _____。
(5)写出一种符合下列条件的乙酰水杨酸的同分异构体的结构简式:。
Ⅰ.能遇FeCl3溶液显紫色Ⅱ.苯环上只有一种一溴取代物
Ⅲ.能发生银镜反应Ⅳ. 1mol该化合物能分别与1molNaOH和2mol金属钠反应
(6) 也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件:
也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件:
。
【化学选修5:有机化学基础】
已知:
有机物A是一种医药中间体,质谱图显示其相对分子质量为130。已知0.5molA完全燃烧只生成3mol CO2和2.5molH2O。A可发生如下图所示的转化,其中D的分子式为C4H6O2,两分子F反应可生成六元环状酯类化合物。
请回答:
(1) A的分子式是。
(2)1mol B与足量的金属钠反应产生22.4L(标准状况)H2。B中所含官能团的名称是。B与C的相对分子质量之差为4,B→C的化学方程式是。
(3) D的同分异构体G所含官能团与D相同,则G的结构简式可能是、。
(4)F可发生多种类型的反应。
①两分子F反应生成的六元环状酯类化合物的结构简式是;
②由F可生成使Br2的CCl4溶液褪色的有机物H。F→H的化学方程式是。
③F在一定条件下发生缩聚反应的化学方程式是。
(5)A的结构简式是。
【化学选修2:化学与技术】工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),其工艺流程如下:
已知:①NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。
②高氯酸是至今为止人们已知酸中的最强酸,沸点90 ℃。
请回答下列问题:
反应器Ⅰ中发生反应的化学方程式为,冷却的目的是,能用蒸馏法分离出高氯酸的原因是。
(2)反应器Ⅱ中发生反应的离子方程式为。
(3)通入反应器Ⅱ中的SO2用H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是 。
(4)Ca(ClO)2、ClO2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,是因为它们都具有,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式:。