下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出),大部分反应在工业生产中得到实际应用。已知Ⅰ、G是单质,且Ⅰ是一种既能与酸反应又能与碱反应生成氢气的金属,L是一种无色气体,K是一种红棕色气体,E是一种红褐色沉淀。
请填写下列空白:
(1)写出下列物质的化学式:C: ;J: 。
(2)写出下列反应的化学反应方程式:
反应⑦: 。
反应⑩: 。
(3)写工业上NH3与O2在一定条件下制取L的化学方程式: 。
某蓝色荧光材料F的合成路线如下:
(1)化合物B中含有的含氧官能团的名称是。
(2)写出化合物CH3NCS的结构式:。
(3)合成路线中属于加成反应的反应有。(填序号)
(4)反应③另一产物为甲醇,其化学方程式为。
(5)与A具有相同的含氮六元环和官能团的同分异构体共有种(包含本身。已知含氮六元环与苯环结构相似)。
(6)已知: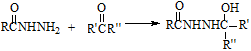 。请写出以
。请写出以 和甲醇为主要原料制备
和甲醇为主要原料制备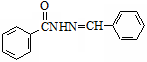 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
CH3CH2OH 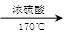 CH2=CH2
CH2=CH2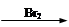 BrCH2—CH2Br
BrCH2—CH2Br
有机物A是分子式为C7H8O2的五元环状化合物,它具有四种不同化学环境的氢,其原子个数比为3:1:2:2它能发生如下转化:
根据以上信息,试回答下列问题:
(1)写出化合物A中官能团的名称。
(2)写出化合物B、F的结构简式BF。
(3)A→B的反应类型是,F→G的反应类型是。
(4)①写出D与CH4O反应的化学方程式。②写出F→G的反应的化学方程式。
(5)写出化合物A的符合下列条件的同分异构体。
①属于芳香族化合物②能与碳酸钠溶液反应③属于醇类化合物
下表为部分短周期元素化合价及其相应原子半径的数据。请回答下列问题:
(1)元素G在周期中的位置是;元素F所形成的常见单质的电子式为。
(2)A、B、C、E的氢化物稳定性顺序是。(用化学式回答)
(3)分子组成为ACH2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是。
(4)请写出B的单质的一种重要用途;工业上制取该单质的原理反应为 。
(5)请设计一个实验方案,使铜和A的最高价氧化物对应的水化物的稀溶液反应,得到蓝色溶液和氢气。请在方框内绘出该实验方案原理装置示意图。
已知:在一定条件下,有如下反应可以发生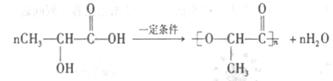
某一试剂瓶的标签严重破损,只能隐约看到下列一部分: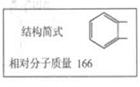
取该试剂瓶中的试剂,通过燃烧实验测得:16.6g该物质完全燃烧得到39.6gCO2与9gH2O。进一步实验可知:①该物质能与碳酸氢钠溶液反应生成无色无味气体。②16.6g该物质与足量金属钠反应可生成氢气2.24L(已折算成标准状况)。请回答:
(1)该有机物的分子式______。该有机物的结构可能______种。
(2)若下列转化中的D是上述有机物可能结构中的一种,且可发生消去反应;E含两个六元环;F是高分子化合物;取C在NaOH水溶液中反应后的混合液,加入足量硝酸酸化后,再加入硝酸银溶液,出现白色沉淀。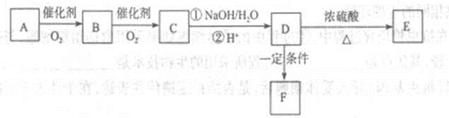
①A的结构简式为____________;
②写出A转化成B的化学方程式____________
③写出由D制取F的化学方程式____________。
④反应类型:D→ E____________
A-E是周期表中1一36号的元素,它们的原子序数依次递增且分别位于前四周期的各个周期中。对它们的性质及结构的描述如下。
A原子的基态只有一种形状的电子云,并容易形成共价键;B原子的最外电子层的电子排布可表示为nsnnpn,其元素最高正化合价与最低负化合价的代数和为0;C与B同周期,其第一电离能髙于周期表中与之相邻的所有元素;D元素在周期表中位于C元素的下一周期,其电负性在同周期元素中最大;E原子最外电子层只有未成对电子,其内层所有轨道全部充满,但并不是第IA族元素。
(1)请写出E原子基态的电子排布式____________。
(2)A与C形成的最简单化合物(甲)分子的立体结构是____________,其中C原子的杂化方式是______
(3)A与D元素形成的化合物(乙)与甲相比,沸点较低的是(写化学式)____________原因是________________________
(4)B元素可形成B70单质,它在一定条件下吸收可见光后可高效杀灭癌细胞,有望成为癌症治疗药物的候选材料。它与金属钾掺杂在一起的化合物,其晶胞如图所示(白球位于立方体的体心和顶点,小黑球位于立方体的面上),则该化合物中B70与钾原子个数比为______。