某蓝色荧光材料F的合成路线如下:
(1)化合物B中含有的含氧官能团的名称是 。
(2)写出化合物CH3NCS的结构式: 。
(3)合成路线中属于加成反应的反应有 。(填序号)
(4)反应③另一产物为甲醇,其化学方程式为 。
(5)与A具有相同的含氮六元环和官能团的同分异构体共有 种(包含本身。已知含氮六元环与苯环结构相似)。
(6)已知: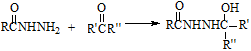 。请写出以
。请写出以 和甲醇为主要原料制备
和甲醇为主要原料制备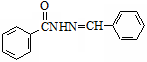 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
CH3CH2OH 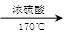 CH2=CH2
CH2=CH2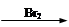 BrCH2—CH2Br
BrCH2—CH2Br
可降解聚合物P的制取路线如下
iii. (还原)其中-NH2基团可以在一定条件下生成-OH基团
(还原)其中-NH2基团可以在一定条件下生成-OH基团
(1)A的含氧官能团名称是_______________。
(2)羧酸a的电离方程是________________。
(3)B→C的化学方程式是________________。
(4)化合物D苯环上的一氯代物有2种,D的结构简式是 。
(5)E→F中反应①和②的反应类型分别是______________、_______________。
(6)F的结构简式是______________。
(7)聚合物P的结构简式是 。
某工厂排放的工业废水中含Fe3+、Al3+、Cu2+,为了减少环境污染,变废为宝,利用废铁屑和其它化学试剂进行如下操作,得到了Fe2O3、Al2O3和金属Cu。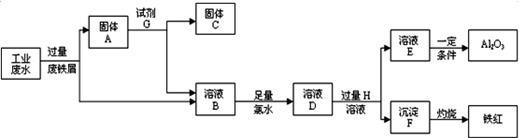
请回答:
(1)固体A的成分是 (用化学式表示)。
(2)溶液B中的金属阳离子有 。
(3)写出下列反应的离子方程式:
B→D: ;
D→E: 。
(4)试剂G是 (写名称);溶液E焰色反应呈紫色(透过蓝色钴玻璃),试剂H是 (用化学式表示)。
已知A是用途最广泛的金属单质,B是常温下呈液态的化合物,E是一种黄绿色的气体。(图中部分产物未标出)。
回答下列问题:
(1)写出F的化学式 。
(2)写出下列反应的化学反应方程式:
反应① ;
反应⑧ 。
(3)写出反应③的离子方程式: 。
(4)鉴别G溶液中阳离子的方法 。
(5)将H溶液滴加到沸水中,继续加热煮沸,得到的液体颜色为 。
我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是某化工厂对海水资源综合利用的示意图:
Ⅰ.(1)写出N的化学式_________________________;
(2)写出反应②的化学方程式_________________________。
Ⅱ.粗盐中含有Ca2+、Mg2+、
SO42-等杂质,精制时所用的
试剂为:①盐酸 ②氯化钡溶液
③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为____________。
A.②③④① B.③④②① C.④③②① D.③②④①
Ⅲ.提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2。
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是____________。
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
(2)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是____________。
A.从外地购买 B.在当地新建生产厂
C.从本厂生产烧碱处循环 D.从本厂生产镁单质处循环
(3)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2 乙:母液先提取Br2,后提取Mg
请你判断哪个更合适?______(填“甲”或“乙),理由是____________________________ ___。
A、B、C、D四种化合物,其中A、C、D均含有钠元素,A、C和盐酸反应均得到D,将固体C加热可得到A,若在A的溶液中通入一种无色无味的气体,又可制得C。若B的溶液滴加到硫酸亚铁溶液中,现象为出现白色沉淀→灰绿色沉淀→红褐色沉淀E。试判断:
(1)A: ___________ E: _____________(写化学式)
(2)①C加热分解的化学方程式_____________________________;
②物质C在水溶液中的电离方程式:__________________________;
③由白色沉淀最终变为红褐色沉淀E的化学方程式________________________________。