醇和酚在人类生产和生活中扮演着重要的角色,根据醇和酚的概念和性质回答下列问题.
(1)下列物质属于醇类的是________.
①CH3CH2CH2OH
②CH3CH(OH)CH3
③CH2===CH—CH2OH
④CH2OH—CH2OH
(2)司机酒后驾车时可检测他呼出的气体,所利用的化学反应如下:
2CrO3(红色)+3C2H5OH+3H2SO4===Cr2(SO4)3(绿色)+3CH3CHO+6H2O
被检测的气体成分是________,上述反应中的氧化剂是________,还原剂是________.
(3)300多年前,著名化学家波义耳发现了铁盐与没食子酸的显色反应,并由此发明了
蓝黑墨水.没食子酸的结构式为: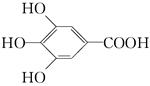 用没食子酸制造墨水主要利用了________类化合物的性质(填代号).
用没食子酸制造墨水主要利用了________类化合物的性质(填代号).
| A.醇 | B.酚 | C.油脂 | D.羧酸 |
依据下列事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。
;
(2)在25℃、101kPa下,若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量。
_______________________________________________________________。
在化学反应中, 只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些
只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些 分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认
分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认 真观察右图,然后回答问题。
真观察右图,然后回答问题。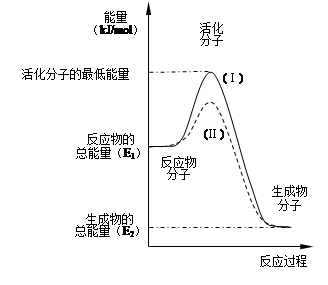
(1)图中所示反应 是_________(填“吸热”或“放热”)反应,该反应的△H =________________(用含E1、E2的
是_________(填“吸热”或“放热”)反应,该反应的△H =________________(用含E1、E2的 代数式表示)。
代数式表示)。
(2)已知热化学方程式:H2(g)+1/2O2(g) = H2O(g) △H =-241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为____________________。
△H =-241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为____________________。
A是一种强酸,其浓度超过40%时就会迅速分解,产生比它的酸性更强的酸B,同时放出气体C和D,该气体经干燥后,平均分子量为47.6,所得气体通过80℃NaOH溶液,得到的产物中一种是A的钠盐,同时还剩余一种可以使带火星的木条复燃的气体D。试完成下列各题:
(1)确定各物质的化学式A________、B________、C________、D____________;
(2)气体C和D的体积比__________ _____;
_____;
(3)写出A分解方程式并配平;;
(4)写出气体C与湿润的淀粉-碘化钾试纸的反应方程式_____________________;
(5)写出将气体C通过80℃NaOH溶液时发生的反应方程式___________________。
已知A为酸式盐,B为某二价主族金属元素的化合物,常温常压下C、D、F、G、I均呈气态。等物质的量A、B与少量的水充分混合能恰好完全反应。图中反应条件(除高温外)均已略去。请回答下列问题:
(1)写出B的电子式,
(2)写出A与B反应的化学方程式。
(3)如对气体 G进行加压操作,产生的现象是。
G进行加压操作,产生的现象是。
(4)写出下列反应的离子方程式:
①在A溶液中加入M。
②向A溶液中加入过量NaOH 溶液,并加热。
溶液,并加热。
化合物A是一种热稳定性较差的无水的弱 酸钠盐。用如下方法对其进行分析:将A与惰性填料混合均匀制成样品,加热至400℃,记录含A量不同的样品的质量损失(%),结果列于下表:利用上述信息和下表中数据,通过作图,推断化合物A的化学式,并给出主要计算过程。
酸钠盐。用如下方法对其进行分析:将A与惰性填料混合均匀制成样品,加热至400℃,记录含A量不同的样品的质量损失(%),结果列于下表:利用上述信息和下表中数据,通过作图,推断化合物A的化学式,并给出主要计算过程。
| 样品中A的质量分数/% |
样品的质量损失/% |
| 20 |
7.4 |
| 50 |
18.5 |
| 70 |
25.8 |
| 90 |
33.3 |