下列各组顺序的排列不正确的是
| A.离子半径:Na+>Mg2+>Al3+>F- |
| B.热稳定性:HCl>H2S>PH3>AsH3 |
| C.酸性强弱:H3AlO3<H2SiO3<H2CO3<H3PO4 |
| D.碱性强弱:KOH>NaOH>Mg(OH)2>Al(OH)3 |
下列离子方程式正确的是
A.过氧化钠与水反应:2O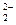 + 2H2O = O2↑ + 4OH + 2H2O = O2↑ + 4OH |
| B.次氯酸钠与Fe(OH)3在碱性溶液中反应生成Na2FeO4: 3ClO  + 2Fe(OH)3 = 2FeO4 + 2Fe(OH)3 = 2FeO4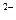 + 3Cl + 3Cl + 4H2O + 4H+ + 4H2O + 4H+ |
C.向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO4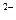 恰好完全沉淀: 恰好完全沉淀:2Al3+ + 3SO4 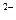 + 3Ba2+ + 6OH + 3Ba2+ + 6OH = 2Al(OH)3↓+ 3BaSO4↓ = 2Al(OH)3↓+ 3BaSO4↓ |
| D.向碳酸氢镁溶液中加入过量的澄清石灰水: |
Mg2+ + 2HCO3 + 2Ca2+ + 4OH
+ 2Ca2+ + 4OH =Mg(OH)2↓+ 2CaCO3↓+ 2H2O
=Mg(OH)2↓+ 2CaCO3↓+ 2H2O
荧光素是发光物质的基质,5-羧基荧光素与5-羧基荧光素二乙酸酯在碱性条件下有强烈的绿色荧光,它们广泛应用于荧光分析等。
5-羧基荧光素(5-FAM) 5-羧基荧光素二乙酸酯(5-CFDA)
下列说法正确的是
A.5-FAM转变为5-CFDA属于取代反应
B.实验室鉴别5-FAM与5-CFDA可用碳酸氢钠溶液
C.5-FAM的分子式为:C21H3O7
D.5-FAM和5-CFDA分子中的所有原子均共面
下列溶液中微粒的物质的量浓度关系正确的是
A.室温下,向0.01mol·L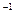 NH4Cl溶液中滴加NaOH溶液至中性: NH4Cl溶液中滴加NaOH溶液至中性:c(Na+) + c(NH4+) + c(H+) = c(OH 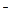 ) + c(Cl ) + c(Cl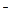 ) ) |
B.0.1 mol·L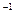 NaHCO3溶液:c(Na+) > c(OH NaHCO3溶液:c(Na+) > c(OH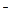 ) > c(HCO3 ) > c(HCO3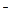 ) > c(H+) ) > c(H+) |
C.Na2CO3溶液:c(OH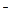 ) = c(HCO3 ) = c(HCO3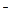 ) + 2c(H2CO3) ) + 2c(H2CO3) |
D.25℃时,pH = 4.75、浓度均为0.1mol·L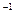 的CH3COOH、CH3COONa混合溶液: 的CH3COOH、CH3COONa混合溶液: |
c(CH3COOH) > c(CH3COO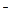 ) > c(H+) > c(OH
) > c(H+) > c(OH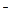 )
)
下列实验操作中,仪器需要插入液面以下的有
①制备Fe(OH)2时用胶头滴管将NaOH溶液滴入FeSO4溶液中;②制备氢气的简易装置中长颈漏斗的下端管口;③石油分馏时所用温度计;④用乙醇制备乙烯时所用温度计:⑤制备乙酸乙酯时,冷凝蒸气的导管。
| A.①②③ | B.②③④ | C.③④⑤ | D.①②④ |
下列说法正确的是
A.某温度时,pH = 6的纯水,含10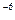 × NA个OH × NA个OH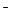 |
B.VL a mol/L的氯化铁溶液中,若Fe3+的数目为NA,则Cl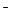 的数目大于3NA 的数目大于3NA |
| C.标准状况下,22.4 LNO和11.2 LO2混合后气体的分子总数为NA |
| D.工业用电解法进行粗铜精炼时,每转移1mol电子,阳极上溶解的铜原子数必为0.5NA |