工业上常用铁质容器盛装冷浓酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
[探究一]已去除表面氧化物的铁钉(碳素钢)放入浓硫酸中,加热,充分反应后收集到气体Y。某同学认为气体Y中除了SO2外还可能含有H2和CO2气体,为此设计了下列实验装置,探究Y中H2和CO2的存在(图中夹持仪器省略)。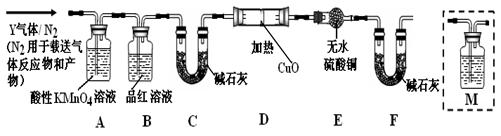
(1)装置B中试剂的作用是 。
(2)认为气体Y中还含有CO2的理由是 (用化学方程式表示)。
(3)为确认CO2的存在,需在装置中添加M于 (选填序号)。
a.. A之前 b . A-B间 c . B-C间 d . C-D间
(4)如果气体Y中含有H2,预计实验现象应是 。
[探究二] SO2气体还原Fe3+、I2,使用的药品和装置如下图所示: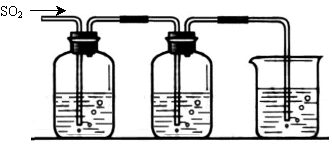
FeCl3溶液 含有淀粉的碘水 NaOH溶液
A B C
(5)装置C的作用是 。
(6)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发浓缩、冷却结晶、 、洗涤、自然干燥,在这一系列操作中没有用到的仪器有 (填序号)。
| A.蒸发皿 | B.石棉网 | C.漏斗 | D.烧杯 E.玻璃棒 F. 坩埚 |
(7)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是 原因是 (8)能表明I-的还原性弱于SO2的现象是 。
下表中每组均有4个选项,请从中选出1个与另三种物质不属于同类的,并注明挑选依据。
| 组别 |
物质 |
不同类 物质序号 |
挑选依据 |
| (1) |
A.HCl B.CO2 C.NH3 D.CaO |
||
| (2) |
A.BaSO4 B.食盐水 C.NaOH D.熔融KCl |
||
| (3) |
A.CO2 B.SO2 C.CO D.P2O5 |
||
| (4) |
A.淀粉溶液 B.蔗糖水C.稀盐酸 D.75%医用酒精 |
某无色溶液里只含有下列8种离子中的某几种:Mg2+、H+、Ag+、Na+、Cl-、HCO3-OH-、NO3-。已知:该溶液能跟金属铝反应,且放出的气体只有氢气。试回答:
(1)若溶液跟铝反应后只有AlO2-生成,则原溶液一定含有的大量物质是,
发生反应的化学方程式是。
还可能含有大量物质是(写化学式)。
(2)若溶液跟铝反应后有Al3+生成,则原溶液中一定不含有的大量离子是。
钛及其合金具有密度小,强度高,耐腐蚀等优良性能,被广泛用于航天、航空、航海、石油化工、医药等部门,因此,钛被誉为第三金属和战略金属。从铁钛矿提取金属钛(海绵钛)的主要工艺过程如下: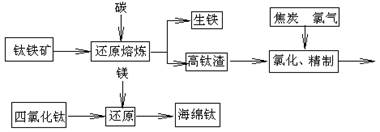
(1)钛铁矿的主要成分是FeTiO3,第一步发生的反应:FeTiO3+C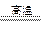 TiO2+Fe+CO↑,在FeTiO3(钛酸亚铁)中,钛的化合价为。
TiO2+Fe+CO↑,在FeTiO3(钛酸亚铁)中,钛的化合价为。
(2)第二步:二氧化钛在高温下与焦炭、氯气反应生成四氯化钛和一氧化碳,写出化学方程式:,还原产物是。
(3)用镁在高温下还原四氯化钛,该反应的环境要求是;写出化学方程式。
(4)菱镁矿(主要成分是碳酸镁)煅烧后与焦炭混合在氯化器中高温下通入氯气生成氯化镁,电解熔融氯化镁得到镁。
①写出菱镁矿煅烧及氯化制取氯化镁的化学方程式:;
②写出电解熔融氯化镁的电解方程式。
相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。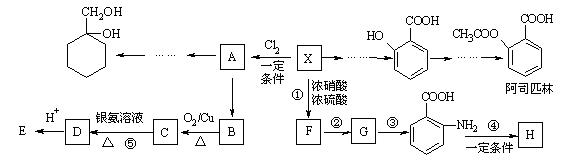
已知:
Ⅰ
Ⅱ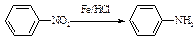 (苯胺,易被氧化)
(苯胺,易被氧化)
请根据所学知识与本题所给信息回答下列问题:
⑴H的结构简式是______________;
⑵反应②的类型是 ;
⑶反应⑤的化学方程式是____________________________________________;
⑷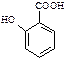 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有________种;
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有________种;
⑸请用合成反应流程图表示出由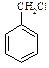 和其他无机物合成
和其他无机物合成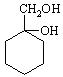 最合理的方案(不超过4步),请在答题纸的方框中表示。
最合理的方案(不超过4步),请在答题纸的方框中表示。 例:
例: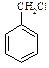

现代社会,铁合金可说是金属材料王国的霸主,铁广泛存在于铁的氧化物及多种矿石中,如下表所示:
| 矿石名称 |
磁铁矿 |
黄铁矿 |
赤铁矿 |
黄铜矿 |
| 主要成分 |
Fe3O4 |
FeS2 |
Fe2O3 |
CuFeS2 |
请回答下列问题:
(1)在上表所列铁的化合物中,铁元素的质量分数含量最高的是。
(2)工业上生产硫酸常以硫铁矿为原料,在沸腾炉中加热使硫元素转化为二氧化硫,其反应的方程式为:4FeS2+11O2 2Fe2O3+8SO2,该反应中被氧化的元素是,生成1molFe2O3转移电子的物质的量为mol。
2Fe2O3+8SO2,该反应中被氧化的元素是,生成1molFe2O3转移电子的物质的量为mol。
(3)生产硫酸的工业尾气中含有大量的SO2,若直接排放到大气中造成环境污染的后
果是,处理该尾气则可得到一种有价值的盐,请写出该盐的名称。
(4)据统计,地球上每年由于腐蚀而消耗的铁约占铁的年产量的10%,铁发生腐蚀的主要原因是(填写下面选项的序号)。
a. 直接与氧气发生了化学腐蚀
b. 通过原电池发生电化学腐蚀
c.与酸雨发生反应而消耗
若你选定选项a或c,请写出相应的化学方程式; 若
你选定选项b,请写出负极的电极反应式。