金属钛被称为铁和铝之后崛起的“第三金属”,常见化合价为+4。它是空间技术、航海、化工、医疗上不可缺少的材料。
工业上用钛铁矿(主要成分FeTiO3)制备金属钛的一种工艺流程如下图(部分产物略去):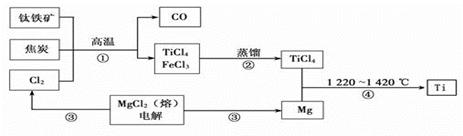
(1)步骤①反应的化学方程式为:2FeTiO3 + 6C + 7Cl2 2FeCl3 + 2TiCl4 + 6CO,还 原剂是 ,每生成1mol TiCl4转移 mol电子。
2FeCl3 + 2TiCl4 + 6CO,还 原剂是 ,每生成1mol TiCl4转移 mol电子。
(2)步骤②分离出TiCl4的方法,利用了TiCl4与FeCl3 的不同。
(3)步骤④反应的化学方程式为______________ __________,该反应在氩气中进行的理由是_________ _____________________。
(4)绿色化学提倡物料循环。以上流程中,可用于循环的物质除Cl2、Mg外,还有___。
某有机物X(C12H13O6Br)分子中含有多种官能团,其结构简式为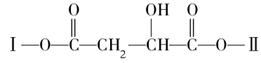
(其中Ⅰ、Ⅱ为未知部分的结构)。为推测X的分子结构,进行如下图的转化: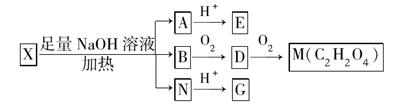
已知向E的水溶液中滴入FeCl3溶液发生显色反应;G、M都能与NaHCO3溶液反应:
(1)M的结构简式是________;G分子所含官能团的名称是________。
(2)E不能发生的反应有(选填序号)________。
| A.加成反应 | B.消去反应 |
| C.氧化反应 | D.取代反应 |
(3)由B转化成D的化学方程式是___________________________。
(4)G在一定条件下发生反应生成分子组成为C4H4O4的有机物(该有机物可使溴的四氯化碳溶液褪色),请写出G发生上述反应的化学方程式____________。
(5)已知在X分子结构中,Ⅰ里含有能与FeCl3溶液发生显色反应的官能团,且E分子中苯环上的一氯代物只有一种,则X的结构简式是________。
(6)F与G互为同分异构体,F的分子中含有羧基、羟基和醛基三种官能团,且同一个碳原子上不能同时连有两个羟基。则F的分子结构有________种。
呋喃酚是合成农药的重要中间体,其合成路线如下: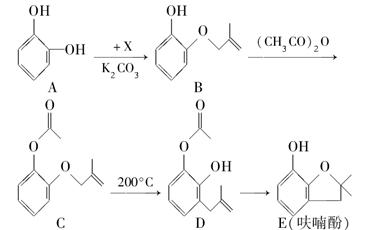
(1)A在空气中久置会由无色转变为棕褐色,其原因是________,A在核磁共振氢谱中有________组峰。
(2)B→C的反应类型是________。
(3)已知X的分子式为C4H7Cl。写出A→B的化学方程式:________________。
(4)要鉴别化合物C和D,适宜的试剂是________。
(5)B的同分异构体很多,符合下列条件的有________种,写出其中能发生银镜反应的同分异构体的结构简式:________(任写一种)。
①苯的衍生物 ②有两个互为对位的取代基 ③含有酯基
乙酸苯甲酯( )广泛存在于可可、咖啡、草莓等物质中,可用作食物和日化用品的香精。
)广泛存在于可可、咖啡、草莓等物质中,可用作食物和日化用品的香精。
已知:X的产量可以用来衡量一个国家的石油化工发展水平,工业上可用X和甲苯人工合成乙酸苯甲酯。其合成路线如下:
据此回答下列问题:
(1)X生成Y的化学方程式为_________________________,生成物Y中含有官能团的名称为_______________________________。
(2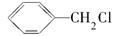 发生反应④所需的条件是____________________,该反应的反应类型为___________________。
发生反应④所需的条件是____________________,该反应的反应类型为___________________。
(3)实验室为鉴别A和B两者的水溶液,可以选用的化学试剂是________。
| A.纯碱溶液 | B.NaOH溶液 | C.金属钠 | D.银氨溶液 |
(4)上述反应①~⑤中原子的理论利用率为100%、符合绿色化学要求的反应是________(填序号)。
(5)请写出反应⑤的化学方程式___________________________________。
(6)写出符合下列条件的乙酸苯甲酯的一种同分异构体:①含苯环结构;②具有酯的结构________。
某种利胆解痉药的有效成分是亮菌甲素,其结构简式如图所示。下列关于亮菌甲素的说法中,正确的是( )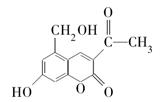
| A.亮菌甲素在一定条件下可以与乙酸发生酯化反应 |
| B.亮菌甲素的分子式为C12H12O5 |
| C.1 mol 亮菌甲素最多能和2 mol NaOH反应 |
| D.1 mol 亮菌甲素最多能和4 mol H2发生加成反应 |
化合物A(C11H8O4)在氢氧化钠溶液中加热反应后再酸化可得到化合物B和C。回答下列问题:
(1)B的分子式为C2H4O2,分子中只有一个官能团。则B的结构简式是________,B与乙醇在浓硫酸催化下加热反应生成D,该反应的化学方程式是________________,该反应的类型是________;写出两种能发生银镜反应的B的同分异构体的结构简式________________;
(2)C是芳香化合物,相对分子质量为180,其碳的质量分数为60.0%,氢的质量分数为4.4%,其余为氧,则C的分子式是________;
(3)已知C的芳环上有三个取代基,其中一个取代基无支链,且含有能使溴的四氯化碳溶液褪色的官能团及能与碳酸氢钠溶液反应放出气体的官能团,则该取代基上的官能团名称是________。另外两个取代基相同,分别位于该取代基的邻位和对位,则C的结构简式是________________;
(4)A的结构简式是___________________。