(10分)普通玻璃是 (混合物、纯净物)玻璃可在一定温度范围内软化,制成工艺品等。这是因为玻璃是一种 物质,没有固定的 。 盛强碱溶液的磨口试剂瓶都不能用玻璃瓶塞的原因是
。
变色眼镜的玻璃片中含有少量的溴化银和微量氧化铜。当玻璃受到阳光照射时,因为发生 反应(用化学方程式表示),而使玻璃由无色变为暗棕色。
2011年5月,台湾传出“毒饮料事件”,一些厂商在饮料中违法添加了“塑化剂”,食品塑化剂事件引起社会的高度关注。常用塑化剂的学名“领苯二甲酸二(2-乙基己)酯”,化学式为C24H38O4,它是一种无色透明的液体,有特殊气味,不溶于水,溶于大多数有机溶剂,有毒。常用作各种塑料制品的工业添加剂,不可食用。可是黑心业者为了牟取暴利,竟然将其添加到多种饮料、果冻、果酱和方便面等食品中。若长期食用此类食品可能对生殖系统、免疫系统造成伤害,大量摄入还可能致癌。
请分析上述信息,回答下列问题:
(1)写出塑化剂的两条物理性质;
(2)下列做法,可以使我们远离塑化剂的是;
①少喝各种饮料,日常饮水以白开水为主
②经常吃方便面、面包等速食食品以适应我们快节奏的生活
③尽量少用塑料制品直接接触热的、含油脂的食物
④呼吁政府完善食品安全监督检验机制,严惩不法黑心业者
(11分)依据氧化还原反应:2Ag+ (aq) + Cu(s) ="=" Cu2+ (aq) + 2Ag (s)设计的原电池如图所示。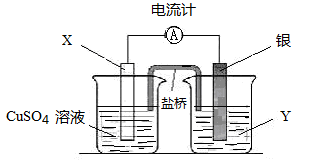
请回答下列问题:
(1)电极X的材料是;电解质溶液Y是;
(2)银电极为电池的极;银电极上发生的电极反应式。
(3)外电路中的电子是从电极流向电极(填电极的材料)。
(4)利用反应Zn + 2 FeCl3 = ZnCl2 + 2 FeCl2,设计一个原电池,在下面框图内画出有关的实验装置图:
正极的电极反应式为。
电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题: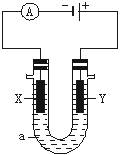
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为。
在X极附近观察到的现象是。
②Y电极上的电极反应式为,
检验该电极反应产物的方法为。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是,电极反应式为。
②Y电极的材料是,电极反应式为。(说明:杂质发生的电极反应不必写出)
(15分)对下图中两极加以必要的连接并填空:
(1)在图A中,使铜片上产生氢气。
①若加以导线连接,则连接后的装置叫(填“原电池”或“电解池”)。锌片发生(填“氧化”或“还原”);铜片上的电极反应式:。
②若外加电源,则连接后的装置叫(填“原电池”或“电解池”),其中铜片作为该装置的极,连接电源的极;锌片上发生的电极反应式为。
(2)在图B中,使a极析出铜。
①若a、b电极均为石墨电极并加以必要的连接,则连接后的装置应为(填“原电池”或“电解池”);该装置工作时,溶液中阴离子向极作定向移动(填“a”或“b”);经过一段时间后,停止反应并搅匀溶液,溶液的酸性(填“增强”、“降低”或“不变”)。
②若a、b电极加以导线连接,且a极为铜电极,则b极可以为电极(填序号)。
| A.铂 | B.铁 | C.石墨 | D.银 E.锌 |
该装置工作时,溶液中阴离子向极作定向移动(填“a”或“b”)。
(8分)已知化学反应中的能量变化,是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同所致。下图为N2(g)和O2(g)生成NO(g)过程中的能量变化: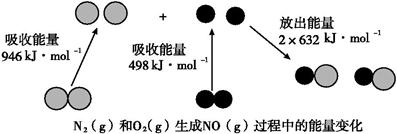
(1)人们通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,则N≡N键的键能为kJ·mol-1。根据上图写出N2(g)和O2(g)生成NO(g)的热化学方程式:。
(2)NO(g)分解生成N2(g)和O2(g)的热化学方程式为:。
当有16 g O2(g)生成时,该反应中放出的热量为:kJ。