已知反应AsO43-+2I-+2H+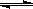 AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。
AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。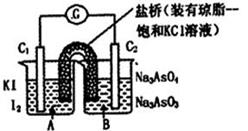
Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40% NaOH溶液
结果发现电流计指针均发生偏转.据此,下列判断正确的是
| A.操作Ⅰ过程中,C1为正极 |
| B.操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液 |
| C.Ⅰ操作过程中,C2棒上发生的反应为:AsO43-+2H++2e - = AsO33-+H2O |
| D.Ⅱ操作过程中,C1棒上发生的反应为:2I- - 2e- = I2 |
下列物质形成的晶体中,其中任何一个原子都被相邻四个原子包围,以共价健形成正四面体,并向空间伸展成网状结构的是
| A.四氯化碳 | B.白磷 | C.金刚石 | D.水晶 |
下列化学用语或模型表示正确的是
A.Cl-离子的结构示意图: |
B.乙醇分子比例模型: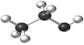 |
| C.次氯酸的结构式:H—O—Cl | D.氢氧化钠的电子式: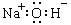 |
化学与科学、技术、社会、环境密切相关。下列有关说法中不正确的是
| A.光缆在信息产业中有广泛应用,制造光缆的主要材料是二氧化硅 |
| B.海轮外壳上镶入铅块,可减缓船体的腐蚀速率 |
| C.大力开发和应用氢能源有利于实现“低碳经济” |
| D.高温能杀死H1Nl流感病毒的原因是蛋白质受热变性 |
一种新燃料电池,一极通入空气,另一极通入丁烷(C4H10)气体,电池的总反应是:
2C4H10 + 13O2 → 8CO2 + 10H2O,电解质溶液是稀H2SO4溶液。下列对该燃料说法正确的是()
| A.在电解质溶液中,SO42-由负极移向正极 |
| B.丁烷在反应过程中被还原 |
| C.通入空气的一极是正极,电极反应为:O2 + 4e- + 4H+ = 2H2O |
| D.通入丁烷的一极是负极,电极反应为:C4H10 + 26e- + 8H2O = 4CO2 + 26 H+ |
丙烷在光照的条件下与氯气混和,生成的二氯代物有几种()
| A.2种 | B.3种 | C.4种 | D.5种 |