下列实验操作、实验现象及解释与结论都正确的是( )
| 编号 |
实验操作 |
实现现象 |
解释与结论 |
| A |
将乙醇与浓硫酸共热至170 ℃,所得气体通入酸性KMnO4溶液中 |
KMnO4溶液褪色 |
乙醇发生消去反应,气体中只含有乙烯 |
| B |
淀粉溶液和稀硫酸混合加热,加新制Cu(OH)2悬浊液 |
有红色沉淀产生 |
淀粉发生水解,产物有还原性 |
| C |
向甲苯中滴入适量浓溴水,振荡、静置 |
溶液上层呈橙红色,下层几乎无色 |
甲苯和溴发生取代反应,使溴水褪色 |
| D |
向蔗糖中加入浓硫酸 |
放热,变黑膨胀,有刺激性气味 |
浓硫酸有脱水性和强氧化性,生成C、SO2和CO2等 |
某溶液中可能含有Na+、NH4+、Ba2+、SO42-、I-、S2-。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是
| A.Na+ | B.SO42- | C.Ba2+ | D.NH4+ |
下列有关实验操作 、现象和解释或结论都正确的是
、现象和解释或结论都正确的是
| 操作 |
现象 |
结论 |
|
| A |
向Na2CO3稀溶液中通入足量CO2 |
溶液变浑浊 |
析出了NaHCO3 |
| B |
向无色溶液中滴加氯水和CCl4,振荡、静置 |
下层溶液显紫色 |
原溶液中有I- |
| C |
Al箔插入稀HNO3中 |
无现象 |
Al箔---表面被HNO3氧化,形成致密的氧化膜 |
| D |
过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 |
溶液呈红色 |
稀HNO3将Fe氧化为Fe3+ |
NaCl是一种化工原料,可以制备一系列物质(见下图)。下列说法正确的是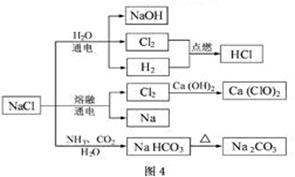
| A.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
| C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D.上图所示转化反应都是氧化还原反应 |
120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是
| A.2.0mol/L | B.1.5 mol/L | C.0.18 mol/L | D.0.24mol/L |
能正确表示下列反应的离子方程式为
A.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S |
| B.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
| C.少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O=C6H5OH+HSO3- |
| D.少量SO2通入到Ba(NO3)2溶液中,正确的离子反应方程式为 |
3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO↑+4H+