用NA表示阿伏加德罗常数,下列叙述正确的是()
| A.1mol Cl2与足量的铁反应,转移的电子数为3NA |
| B.在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA |
| C.3.4gH2O2中含有的共用电子对数为0.1NA |
| D.标准状况下,lmol SO3含有的氧原子数为3NA |
下列有关实验原理或实验操作正确的是()
| A.用pH试纸测定氯水的pH |
| B.过滤时为了加快过滤速度,可以用玻璃棒小心搅拌 |
C.选择合适的试剂,用右图所示装置可分别制取少量CO2和O2 |
| D.室温下向苯和苯酚的混合溶液中加入浓溴水,充分反应后过滤,可除去苯中少量苯酚 |
下列表示对应化学反应的离子方程式正确的是()
| A.漂白粉溶液中通入过量二氧化碳: Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO |
| B.NaOH溶液中滴人饱和FeCl3溶液: Fe3++3H2O 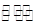 3H++3Fe(OH)3(胶体) 3H++3Fe(OH)3(胶体) |
C.将氯气溶于水配制氯水:Cl2+H2O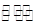 H++Cl-+HClO H++Cl-+HClO |
| D.用硫酸酸化的KMnO4溶液与H2O2反应: |
2MnO4-+10H++3H2O2=2Mn2++3O2↑+8H2O
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g·L-1,W在短周期主族元素中原子半径最大。下列说法正确的是()
| A.原子半径:Z>Y>X |
| B.M2Z能与W的单质发生反应 |
| C.由X元素形成的单质一定是原子晶体 |
| D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
下列各组离子在指定溶液中能大量共存的是()
①常温下,c(H+)/c(OH一)=1×10-12的溶液:K+、AlO2-、CO32-、Na+
②加入苯酚显紫色的溶液:K+、NH4+、Cl-、I一
③中性溶液:Fe3+、Al3+、NO3-、SO42-
④使pH试纸变蓝的溶液中:Al3+、Na +、SO42-、Cl一
+、SO42-、Cl一
⑤无色溶液中:K+、Al3+、NO3-、HCO3-
| A.②③ | B.①③ | C.① | D.①④⑤ |