聚合硫酸铁又称聚铁, 化学式为[Fe(OH)(SO4)]m, 广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O )过程如下: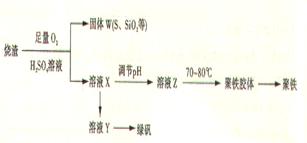
验证固体W焙烧后产生的气体含有SO2的方法是
(2)实验室制备、收集干燥的SO2, 所需仪器如下。装置A产生SO2, 按气流方向连接各仪器接口,顺序为a→___ →___ →___ →___f。装置D的作用是 , 装置E中NaOH溶液的作用是 。 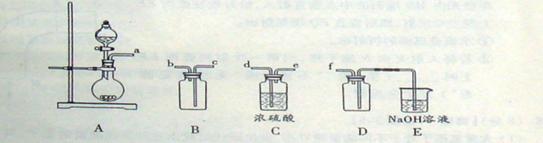
(3)制备绿矾时,向溶液X中加入过量_____,充分反应后,经_______操作得到溶液Y,再经浓缩,结晶等步骤得到绿矾。
(4)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH的操作方法为 。若溶液Z的pH偏小,将导致聚铁中铁的质量分数偏_______。
【选修2—化学与技术】水处理技术在生产、生活中应用广泛。
(1)工业上常用绿矾做混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理的水pH调到9左右,再加入绿矾。请解释这一做法的原因:_________。(用必要的离子方程式和文字描述)。
(2)根据水中Ca2+,Mg2+的多少,把天然水分为硬水和软水,硬水必须经过软化才能使用。
①硬水软化的方法通常有___________、__________和离子交换法。离子交换树脂使用了一段时间后,逐渐由NaR型变为CaR2(或MgR2)型,而失去交换能力。把CaR2(或MgR2)型树酯置于______________中浸泡一段时间,便可再生。
②当洗涤用水硬度较大时,洗衣粉与肥皂相比,___________洗涤效果较好,原因是______________。
(3)最近我国某地苯胺大量泄漏于生活饮用水的河道中,当地采取的应急措施之一是向河水中撒入大量的活性炭,活性炭的作用是___________________。
(4)若生活污水中含大量氮化合物,通常用生物膜脱氮工艺进行处理。首先在消化细菌作用下将 氧化为
氧化为 :_____
:_____ +______O2=______
+______O2=______ +_____H++______H2O。然后加入甲醇与
+_____H++______H2O。然后加入甲醇与 生成N2:______
生成N2:______ +______CH3OH=_______N2+______CO2+_________H2O+_______OH-(试配平以上两个离子方程式)。
+______CH3OH=_______N2+______CO2+_________H2O+_______OH-(试配平以上两个离子方程式)。
(1)常温下,向20 mL 0.2 mol·L-1H2A溶液中滴加0.2 mol·L-1NaOH溶液。有关微粒物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)。请根据图示填空:
①当V(NaOH)=20mL时,溶液中离子浓度的大小关系: ___________________;
②等体积、等物质的量浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水_________(填“大”、“小”或“相等”),欲使NaHA溶液呈中性,可以向其中加入___________。
(2)氨气分解反应的热化学方程式如下:2NH3(g) N2(g)+3H2(g) △H=+92.4kJ·mol-1研究表明金属催化剂可加速氨气的分解。图1为某温度下等质量的不同金属分别催化等浓度氨气分解生成氢气的初始速率。
N2(g)+3H2(g) △H=+92.4kJ·mol-1研究表明金属催化剂可加速氨气的分解。图1为某温度下等质量的不同金属分别催化等浓度氨气分解生成氢气的初始速率。
①不同催化剂存在下,氨气分解反应的活化能最大的是__________(填写催化剂的化学式)。
②恒温(T1)恒容时,用Ni催化分解初始浓度为c0的氨气,并实时监测分解过程中氨气的浓度。计算后得氨气的转化率α(NH3)随时间t变化的关系曲线(见图2)。请在图2中画出:如果将反应温度提高到T2,Ru催化分解初始浓度为c0的氨气过程中α(NH3)—t的总趋势曲线(标注Ru—T2)
③假设Ru催化下温度为T1时氨气分解的平衡转化率为40%,则该温度下此分解反应的平衡常数K与c0的关系式是:K=_____________。
物质的类别和核心元素的化合价是研究物质性质的两个基本视角。
(1)图中X的电子式为;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O(填“强”或“弱”)。用原子结构解释原因:同主族元素最外层电子数相同,从上到下,,得电子能力逐渐减弱。
(2)Na2S2O3是一种用途广泛的钠盐。
①下列物质用于Na2S2O3的制备,从氧化还原反应的角度,理论上有可能的是______(填字母序号)。
a. Na2S+ S b. Z+ S c. Na2SO3 + Y d. NaHS + NaHSO3
②已知反应:Na2S2O3 + H2SO4 ="=" Na2SO4 + S↓+SO2↑+H2O。研究其反应速率时,下列说法正确的是(填写字母序号)。
a.可通过测定一段时间内生成SO2的体积,得出该反应的速率
b.可通过比较出现浑浊的时间,研究浓度、温度等因素对该反应速率的影响
c.可通过Na2S2O3固体与稀硫酸和浓硫酸的反应,研究浓度对该反应速率的影响
(3)治理含CO、SO2的烟道气,可以将其在催化剂作用下转化为单质S和无毒的气体。
已知:①CO(g)+ 1/2 O2(g)=CO2(g)△H=-283 kJ·mol-1
②S(s)+ O2(g)=SO2(g)△H=-296 kJ·mol-1
①则治理烟道气反应的热化学方程式为。
②一定条件下,将CO与SO2以体积比为4∶1置于恒容密闭容器中发生上述反应,下列选项能说明反应达到平衡状态的是(填写字母序号)。
a.v (CO) ∶v(SO2) = 2∶1
b.平衡常数不变
c.气体密度不变
d.CO2和SO2的体积比保持不变
测得上述反应达平衡时,混合气体中CO的体积分数为 ,则SO2的转化率为。
,则SO2的转化率为。
铁、铜及其化合物在工农业生产中应用广泛。
(1)在潮湿空气中,钢铁发生电化学腐蚀转化为Fe(OH)2的反应方程式为。在含有等浓度硫酸溶液的下列装置中,铁腐蚀的速率由快到慢的顺序是(用序号填写)。
(2)已知:①3Fe(s)+2O2(g)=Fe3O4(s) H="-1118" kJ·mol-1
H="-1118" kJ·mol-1
②2Al(s)+3/2O2(g)=A12O3(s) H="-1675.7" kJ·mol-1
H="-1675.7" kJ·mol-1
则焊接钢轨时铝与Fe3O4发生反应生成铁和Al2O3的热化学方程式为。
(3)Na2FeO4具有强氧化性,其电解制法如图所示,请写出阳极的电极反应式。Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其原理是。
(4)工业上常用FeCl3溶液腐蚀印刷线路板,发生反应的离子方程式是。若腐蚀铜板后的溶液中,Cu2+、Fe3+和Fe2+浓度均为0.1 mol·L-1,结合下图分析,当混合溶液中通入氨气调节溶液的pH=5.6时,溶液中存在的金属阳离子为。从图中数据计算Fe(OH)2的溶度积Ksp[Fe(OH)2]=。
已知:横坐标为溶液的pH,纵坐标为金属离子的物质的量浓度的对数(当溶液中金属离子浓度 10-5 mol·L-1时,可认为沉淀完全)。
10-5 mol·L-1时,可认为沉淀完全)。
利用天然气可制得以H2、CO等为主要组成的工业原料合成气,反应为:CH4(g)+H2O(g) CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)甲烷与水蒸气反应,被氧化的元素是,当生成标准状况下35.84L合成气时转移电子的物质的量是。
(2)将2 mol CH4和5 mol H2O(g)通入容积为100L的反应室,CH4的平衡转化率与温度、压强的关系如图。
①达到A点所需的时间为5min,则v(H2)=,100℃时平衡常数K=。
②图中的Pl P2(填“<”、“>”或“=”),A、B、C三点的平衡常数KA、KB、KC的大小关系是。
(3)合成气用于合成氨气时需除去CO,发生反应CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g) H<0,
H<0,
下列措施中能使 增大的(选填编号)。
增大的(选填编号)。
A.降低温度B.恒温恒容下充入He(g)
C.将H2从体系中分离D.再通入一定量的水蒸气
可用碳酸钾溶液吸收生成的CO2,常温下pH=10的碳酸钾溶液中水电离的OH-的物质的量浓度为,常温下,0.1 mol·L-1KHCO3溶液pH>8,则溶液中c(H2CO3)c(CO32-)(填“>”、“=”或“<”)。