相同条件下,在容积相同的三个烧瓶内分别充满干燥的NH3、HCl、NO2气体,做喷泉实验,所得三种溶液的物质的量浓度比为
| A.3 :3 :2 | B.2 :2 :3 | C.1 :1 :1 | D.无法比较 |
下列各组元素递变情况错误的是 ( )
A. Li、Be、B 原子最外层电子数依次增多
B. P、S、Cl 元素最高正化合价依次升高
C. B、C、N、O、F原子半径依次增大
D. Li、Na、K、Rb的金属性依次增强
某元素最高正价和负价的绝对值相等,氧化物和氢化物在常温下均为气态,该元素是()
| A.硅 | B.氮 | C.碳 | D.硫 |
向50mL 18mol/L H2SO4溶液中加入足量的铜片并加热。充分反应后,被还原的H2SO4的物质的量()
| A.大于0.90mol | B.等于0.45mol |
| C.在0.45mol和0.90mol之间 | D.小于0.45mol |
在下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,但未能充满烧瓶。则a和b分别是()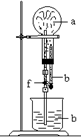
| a(干燥气体) |
b(液体) |
|
| A. |
NO2 |
水 |
| B. |
CO2 |
4mol·L-1NaOH溶液 |
| C. |
Cl2 |
饱和NaCl水溶液 |
| D. |
NH3 |
1mol·L-1盐酸 |
实验室常将浓盐酸与浓硫酸混合来制备HCl气体,下列与该原理无关的是()
| A.浓硫酸具有脱水性 | B.浓硫酸具有吸水性 |
| C.浓硫酸稀释放热 | D.气体在水中的溶解度随温度升高而减小 |