下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径/nm |
0.160 |
0.134 |
0.089 |
0.102 |
0.074 |
| 主要化合价 |
+2 |
+3 |
+2 |
+6、-2 |
-2 |
A. 与
与 的核外电子数相等
的核外电子数相等
B.L与T形成的化合物具有两性
C.氢化物的稳定性为
D.单质与浓度相等的稀盐酸反应的速率为Q<L
苯不能使少量酸性高锰酸钾溶液褪色,但苯的同系物能使少量酸性高锰酸钾溶液褪色,下列解释正确的是()
| A.苯的同系物中原子数比苯分子中原子数多 | B.苯环受侧链的影响而易被KMnO4氧化 |
| C.侧链受苯环的影响而易被KMnO4氧化 | D.苯环和侧链相互影响,同时被氧化 |
下列烷烃的命名正确的是()
| A.2,4-二乙基戊烷 | B.4-甲基-3-乙基已烷 |
| C.2-甲基-3-丙基戊烷 | D.2,3,3-三甲基戊烷 |
含一个叁键的炔烃,和氢气充分加成后的产物的结构简式为: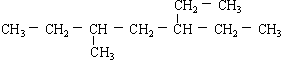 ,此炔烃可能有的结构有()
,此炔烃可能有的结构有()
| A.1种 | B.2种 | C.3种 | D.4种 |
下列说法不正确的是( )
| A.同系物的化学性质相似 |
| B.同位素的化学性质几乎相同 |
| C.相对分子质量相同的化合物,互称同分异构体 |
| D.同素异形体之间的转化,同分异构体之间的转化都属于化学变化 |
下列化学式中只能表示一种物质的是()
| A.C3H7Cl | B.CH2Cl2 | C.C2H6O | D.C2H4O2 |