由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱溶液反应制得Fe(OH)2白色沉淀。若用左图所示实验装置,则可制得纯净的Fe(OH)2白色沉淀。已知两极材料分别为石墨和铁: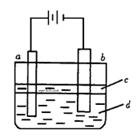
(1)a极材料为 ,电极反应式为 。
(2)电解液d可以是 ,则白色沉淀在电极上生成;电解液d也可
以是 ,则白色沉淀在两极间的溶液中生成。
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)液体c为苯,其作用是 ,在加苯之前对d溶液
进行加热煮沸处理,目的是 。
(4)为了在短时间内看到白色沉淀,可以采取的措施是 。
A.改用H2SO4作电解液 B.适当增大电源电压
C.适当缩小两极间距离 D.适当地降低电解液的温度
(5)若d改为Na2SO4溶液,当电解一段时间,看到白色沉淀后,再反接电源继续电解,除了电极上看到的气泡外,另一明显的现象为 。
X、Z、Q、R 4种短周期元素原子序数的依次增大,Y是一种短周期主族非金属元素。化合物甲由X、Z、Q 3种元素组成,常温下,0.1mol·L-1甲溶液的pH=13。工业上常用电解QR饱和溶液生产甲。请填写下列空白。
(1)Q的原子结构示意图为。
(2)电解QR饱和溶液反应的离子方程式为。
(3)常温下将R的单质通入甲溶液中,发生反应的离子方程式为。
(4)①若Y与X组成的气体化合物乙在常温下遇XR气体时产生白烟,则乙的化学式为;YZ2与水反应的化学方程式:________________________________________
②若Y元素的单质能发生如图所示转化,则Y元素名称是。YZ2的结构式为:_____________YZ2通过置换反应可生成Y的单质,该反应式为:____________________________________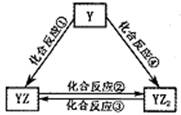
③若Y元素的单质是一种淡黄色固体。写出Y的最高价氧化物的水化物的浓溶液与铜共热的化学方程式:______________ ____________________________________
④若Y的最高价氧化物可制光导纤维。写出工业生产Y单质的反应的化学方程式:____________________________________________________________
已知化合物A和金属单质B反应生成C和D的同时放出大量的热;若将F的饱和溶液滴入沸水中,煮沸可得到以H为分散质的红褐色液体。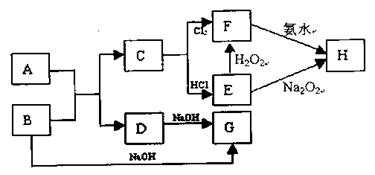
请回答下列问题:
(1)红褐色液体中H粒子的直径大小范围。
(2)写出D、E的化学式:D、E
(3)写出H2O2的电子式:,及E的酸性溶液与双氧水反应的离子方程式。
(4)写出B→G反应的化学方程式:
(5)写出F溶液中阳离子检验方法:
离子方程式为。
.实验室中用Cu和稀HNO3反应制取NO,反应的方程式是:
。
反应中被氧化的物质是,被还原的元素是,
氧化产物是,还原产物是,氧化剂与还原剂的物质的量之比是,硝酸所表现的性质是。
(10分)X、Y、Z为三个不同短周期非金属元素的单质。在一定条件下有如下反应:
Y+X→A(g),Y+Z→B(g)请针对以下两种不同情况回答:
(1)若常温下X、Y、Z均为气体,且A和B化合生成固体C时有白烟产生,则:
①Y的化学式是。
(2)若常温下Y为淡黄色固体,X、Z为气体,B可把A氧化为Y,则:
①B的化学式是;
②向苛性钠溶液中通入过量的A,所发生反应的离子方程式是
③将Y与(1)中某单质的水溶液充分反应可生成两种强酸,该反应的化学方程式是
(12分)A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周期;E元素原子的最外层电子数比次外层电于数少2;A、B、D、E这四种元素,每一种与C元素都能形成原子个数比不相同的若于种化合物。请回答:
(l)B元素的名称是。在周期表中的位置是。
(2)C和E两种元素相比较,原子得电子能力较强的是(填元素名称)。
以下三种说法中,可以验证该结论的是(填写编号) 。
A.比较这两种元素的常见单质的沸点
B.二者形成的化合物中,C元素的原子显负价
C.比较这两种元素的气态氢化物的稳定性
(3)A、B、C、E可形成两种酸式盐(均含有该四种元素),这两种酸式盐在水溶液中相互反应的离子方程式为。
(4)C与D形成的某种化合物可作潜水面具中的供氧剂,每生成标准状况下11.2LO2,消耗该化合物的质量为。