碳、硅元素的单质及其化合物是构成自然界的重要物质。
(1)甲烷是最简单的有机物,实验室可通过下列反应制取:CH3COONa+NaOH CH4↑+X(已配平)
CH4↑+X(已配平)
①X属于 晶体(填晶体类型)。
②MgO晶体的熔点比CaO高,主要原因是 。
(2)金刚石和石墨是两种重要的碳单质。
①以Ni—Cr—Fe为催化剂,一定条件下可将石墨转化为金刚石。基态Cr3+离子中未成对电子数有 个。
②石墨晶体具有层状结构,在层与层之间嵌入金属K原子,能形成石墨夹层离子化合物(KC8),KC8固态时也能导电,导电的粒子是 。
(3)硅烷(SiH4)的结构与甲烷相似。SiH4分子中共价键的类型是 ;硅烷能与硝酸银发生如下反应:SiH4+8 AgNO3+2 H2O =" 8" Ag↓+SiO2↓+8 HNO3
该反应中氢元素被氧化,由此可判断电负性:Si H(填“>”、“<”或“=”)
(4)下图中,能正确表示与Si同周期部分元素的第三电离能(I3)与原子序数关系的
是 (填标号)。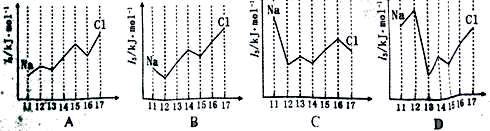
硫在自然界中以游离态和多种化合态形成出现。硫的化合物大多具有氧化性或还原性。许多金属硫化物难溶于水。
完成下列填空:
(1)硫化氢具有还原性,可以和许多氧化剂反应。在酸性条件下,
和
反应生成
、
、
和
,写出该反应的化学方程式。
(2)石油化工的废气中有
。写出从废气中回收单质硫的两种方法(除空气外,不使用其他原料),以化学方程式表示。、
(3)室温下,0.1
的硫化钠溶液和0.1
的碳酸钠溶液,碱性更强的是,其原因是。
已知:
:
=1.3×10-7
=7.1×10-15
:
=4.3×10-7
=5.6×10-11
(4)向
溶液中滴加饱和
溶液,没有沉淀生成,继续滴加一定量的氨水后,生成
沉淀。用电离平衡原理解释上述现象。
(5)将黑色的 固体加入足量盐酸中,溶液中有淡黄色固体生成,产物还有、。过滤,微热滤液,然后加入过量的氢氧化钠溶液,可观察到的现象是。
合成氨工艺的一个重要工序是铜洗,其目的是用铜液[醋酸二氨合铜(I)、氨水]吸收在生产过程中产生的
和
等气体。铜液吸收
的反应是放热反应,其反应方程式为:
完成下列填空:
(1)如果要提高上述反应的反应速率,可以采取的措施是。(选填编号)
a.减压 b.增加NH3的浓度 c.升温 d.及时移走产物
(2)铜液中的氨可吸收二氧化碳,写出该反应的化学方程式。
(3)简述铜液吸收
及铜液再生的操作步骤(注明吸收和再生的条件)。
(4)铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为。其中氮元素原子最外层电子排布的轨道表达式是。通过比较可判断氮、磷两种非金属元素的非金属性强弱。
(5)已知
与
分子结构相似,
的电子式是。
熔点高于
,其原因是。
3﹣对甲苯丙烯酸甲酯(
)是一种用于合成抗血栓药的中间体,其合成路线如下:
已知:
(1)遇
溶液显紫色且苯环上有两个取代基的
的同分异构体有种,
中含氧官能团的名称为.
(2)试剂
可选用下列中的.
a、溴水
b、银氨溶液
c、酸性
溶液
d、新制
悬浊液
(3)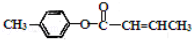 是
的一种同分异构体,该物质与足量
溶液共热的化学方程式为.
是
的一种同分异构体,该物质与足量
溶液共热的化学方程式为.
(4)
在一定条件下可以生成高聚物
,
的结构简式为.
【化学-物质结构与性质】
石墨烯(如图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(如图乙).
(1)图甲中,1号C与相邻C形成σ键的个数为.
(2)图乙中,1号C的杂化方式是,该C与相邻C形成的键角(填">""<"或"=")图甲中1号C与相邻C形成的键角.
(3)若将图乙所示的氧化石墨烯分散在H2O中,则氧化石墨烯中可与H2O形成氢键的原子有(填元素符号).
(4)石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部,该晶胞中M原子的个数为,该材料的化学式为.
离子液体是一种室温熔融盐,为非水体系,由有机阳离子、
和
组成的离子液体作电解液时,可在钢制品上电镀铝。
(1)钢制品应接电源的极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为。若改用
水溶液作电解液,则阴极产物为。
(2)为测定镀层厚度,用
溶液溶解钢制品表面的铝镀层,当反应转移6
电子时,所得还原产物的物质的量为
。
(3)用铝粉和
做铝热反应实验,需要的试剂还有。
.
.
.
.
取少量铝热反应所得到的固体混合物,将其溶于足量稀 ,滴加 溶液无明显现象,(填"能"或"不能")说明固体混合物中无 ,理由是(用离子方程式说明)。