如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的不可能是 ( )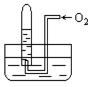
| A.N2与NO2的混和气体 | B.O2与NO2的混和气体 |
| C.NO与NO2的混和气体 | D.NO2一种气体 |
美国航天局宣布,月球坑观测和传感卫星获得的撞月数据显示,月球上存在“数量可观的水”。下列有关说法正确的是()
A.月球上的H2O分子中只含有非极性共价键
B.H2O在化学反应中既可作氧化剂又可作还原剂
C.氢的三种同位素H、D、T与16O只能形成三种水分子
D.在标准状况下,1mol水的体积约是22.4L
下列变化过程,属于放热反应的是 ( )
①生石灰与水反应;②NH4Cl晶体与Ba(OH)2·8H2O混合搅拌;③醋酸电离;④固体氢氧化钠溶于水;⑤H2在Cl2中燃烧;⑥浓H2SO4稀释;⑦酸碱中和反应
| A.①②⑤ | B.①⑤⑦ | C.①④⑤⑥⑦ | D.③⑥⑦ |
下列化学用语正确的是()
| A.CaH2的电子式:[H:]_Ca2+[:H]- | B.铝离子的结构示意图: |
C.CO2的比例模型: |
D.核内有8个中子的碳原子: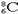 |
化学与生活密切相关,下列说法不正确的是()
| A.风能、生物质能、沼气是可再生能源,煤、石油、天然气是不可再生能源 |
| B.“84消毒液”具有强氧化性,可做环境的消毒剂从而预防流感 |
| C.雾霾天气严重影响人类健康,PM2.5是指大气中直径小于或者等于2.5微米的颗粒物,也称为“细颗粒物”PM2.5在空气中可能形成胶体。 |
| D.已知水热反应是指在高温高压下,将二氧化碳转化为有机物的技术,可以降低自然界中碳的含量 |
有五瓶失去标签的无色溶液A,B,C,D,E分别为氢氧化钠溶液、硫酸钠溶液、硝酸钠溶液、氯化钠溶液和碳酸钠溶液。为把它们一一鉴别开,按下面的实验步骤进行:
(1)分别取五种溶液少许,加入无色试剂X,A、B、E三种溶液无变化,C、D溶液中有白色沉淀生成。
(2)分别另取五种溶液少许,加入无色酚酞试液,A、B、C三种溶液无变化,D、E两种溶液显红色。
(3)分别另取五种溶液少许,加入无色试剂Y,A、B、C、E四种溶液均无变化,D溶液中有气泡生成。
(4)分别取A、B两种溶液,各滴入AgNO3溶液,A中有白色沉淀生成。
回答下列问题:①确定A、B、C、D、E各是什么溶液。
A为_______溶液,B为________溶液,C为_________溶液,D为_________溶液,E为_______溶液
②所加试剂X、Y各是什么溶液。试剂X为___________溶液,试剂Y为___________溶液