下列化学用语正确的是( )
| A.CaH2的电子式:[H:]_Ca2+[:H]- | B.铝离子的结构示意图: |
C.CO2的比例模型: |
D.核内有8个中子的碳原子: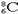 |
下列有关热化学方程式的说法中正确的是()
| A.热化学方程式未注明温度和压强时,ΔH表示标准状况下的数据 |
| B.热化学方程式中的化学计量数只代表反应物或生成物的物质的量 |
| C.在加热条件下进行的反应一定是吸热反应 |
| D.同一化学反应反应条件不同,ΔH值一定不同 |
下列对化学反应的认识错误的是()
| A.会引起化学键的变化 | B.会产生新的物质 |
| C.必然引起物质状态的变化 | D.必然伴随着能量的变化 |
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是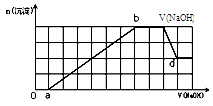
A.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
B.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓, Mg2++2OH-= Mg(OH)2↓
C.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+[、Na+
D.d点溶液中含有的溶质只有Na2SO4
家蝇的雌性信息素可用芥酸(来自菜籽油)与羧酸X在浓NaOH溶液中进行阳极氧化得到。电解总反应式为:
则下列说法错误的是
| A.X的结构简式为C2H5COOH |
| B.电解的阳极反应式为:C21H41COOH+X+ 6OH--2e-→C23H46+2CO32-+4H2O |
| C.该反应中所有碳原子均被氧化,每转移1mole-生成0.5mol雌性信息素 |
| D.阴极的还原产物为H2 |
实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体经历下列过程(Fe3+在pH=5时已完全沉淀):
下列分析正确的是
| A.用98%的浓硫酸配制溶解所用的4.5 mol·L-1的稀硫酸,只需3种玻璃仪器 |
| B.步骤②目的是将溶液Ⅰ中的Fe2+充分转化成Fe3+,实验操作是向溶液Ⅰ中通入足量的氯气 |
| C.利用Cu(OH)2替代CuO也可调节溶液pH而不影响实验结果 |
| D.步骤④之后的实验操作是蒸干溶剂结晶,所需仪器是蒸发皿、玻璃棒、酒精灯、泥三角、三脚架 |