下列说法正确的是()
| A.控制塑料购物袋的使用主要是为了节约成本 |
| B.使用可降解塑料袋有利于减少“白色污染” |
| C.聚氯乙烯塑料袋可用来长时间存放食品 |
| D.塑料购物袋具有热固性,不能回收利用 |
下列说法不正确的是
| A.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,PM2.5比胶体粒子小,因其比表面积大,故可吸附重金属离子,入肺后对人体产生很大的危害 |
| B.红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析 |
| C.石油催化裂化的主要目的是提高汽油等轻质油的产量与质量;石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃 |
| D.阴极射线和α-粒子散射现象都对原子结构模型的建立做出了贡献 |
有一无色溶液,可能含有K+、Ag+、Al3+、Mg2+、NH4+、Cl-、SO32- 、SO42-、I-、Br-、HCO3-、AlO2-、MnO4-中的几种。为确定其成分,做如下实验:
①取少量原溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀;再加热,未见有气体放出;
②重新取少量原溶液,滴加适量的饱和氯水,有气泡生成,溶液呈现橙黄色;加入四氯化碳振荡、静置,四氯化碳层呈橙红色;分液后,向水层加入BaCl2溶液,有白色沉淀产生。下列推断正确的是
| A.肯定有Al3+、Mg2+、NH4+、SO32- 、Br- |
| B.肯定有Mg2+、Br-、HCO3-、SO42- |
| C.肯定无Ag+、Cl-、I-、AlO2-、MnO4- |
| D.可能有K+、Cl-、SO42-、I- |
常温下,用0.1000 mol•L-1 NaOH溶液滴定 20.00 mL 0.1000 mol•L-1 CH3COOH溶液滴定曲线如上右图。下列说法正确的是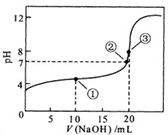
| A.点①所示溶液中:c(CH3COO-)+ c(OH-)= c(CH3COOH)+ c(H+) |
| B.点②所示溶液中:c(Na+)= c(CH3COOH)+ c(CH3COO-) |
| C.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| D.滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)] |
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6 g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是
| A.原混合酸中HNO3的物质的量为0.1 mol |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+ = 3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4浓度为2.5 mol·L-1 |
Li-Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:2Li++FeS+2e═Li2S+Fe ,有关该电池的下列中,正确的是
| A.Li-Al在电池中作为负极材料,该材料中Li的化合价为+1价 |
| B.该电池的电池反应式为:2Li + FeS = Li2S + Fe |
| C.负极的电极反应式为Al-3e-=Al3+ |
| D.充电时,阴极发生的电极反应式为:Li2S + Fe -2e- = 2Li+ + FeS |