X、Y、Z、E、F为五种短周期元素,原子序数依次递增。X+只含有一个质子;Y的最高正化合价、最低负化合价绝对值相等,在同族元素中其氢化物最稳定;Z的原子核内质子数是Y的最外层电子数的2倍;F与Z同主族;E与X同主族。试推断
(1)下列元素分别是:Y__________、Z____________、F__________。(用元素符号表示)
(2)其中原子半径最大的元素是 ,原子半径最小的元素是 .(填元素符号)
(3)X、Z、E形成化合物的电子式为________,所含有的化学键有________;它属于________化合物(填“离子”或“共价”)。
W、X、Y、Z是短周期主族元素,它们的核电荷数依次增大。下表列出它们的性质和结构:
| 元素编号 |
元素性质或原子结构 |
| W |
原子电子层数与核外电子数相等 |
| X |
原子核外L层上s能级的电子总数为p能级上的电子总数的一半 |
| Y |
元素的原子半径在短周期中最大(除稀有气体外) |
| Z |
原子核外p能级上的电子总数等于s能级上的电子总数 |
(1)W和X按1︰1形成的化合物的电子式为 ,晶体Z属于 晶体。
(2)Y元素的单质在W和X按2︰1形成的化合物中反应的离子方程式为。
(3)Z和CO2在一定条件下反应的化学方程式为 。
氮元素可以形成多种化合物。
(1)基态氮原子的价电子轨道表示式是 。
(2)已知尿素的结构式为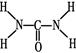 ,则尿素分子中C和N原子的杂化方式分别是、。
,则尿素分子中C和N原子的杂化方式分别是、。
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮化物。
①NH3分子的空间构型是;
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g)△H=-1038.7kJ·mol-1
当肼燃烧放出519.35kJ热量时,形成的π键有mol。
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
| a |
|||||||
| b |
c |
d |

(1)元素b的基态原子电子排布式为 。
(2)第三周期8种元素按单质熔点高低的排列顺序如右图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号)。
(3)元素a、c分别与元素d形成的化合物中,熔点较高的是(填化学式)。
卤族元素包括F、Cl、Br、I等。
(1)下列曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是 (填写序号)。
(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷。
①下图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为 ,
该功能陶瓷的化学式为 ;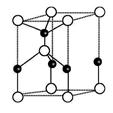
②第一电离能介于B、N之间的第二周期元素有 种。
(3)ZnCl2与氨水反应可形成配合物[Zn(NH3)4]Cl2,1mol该配合物中含有σ键的物质的量为 。
(1)下列7种物质:
①白磷(P4) ②水晶 ③氯化铵 ④氢氧化钙 ⑤氟化钠 ⑥过氧化钠 ⑦干冰
固态时都为晶体,其中既有范德华力,又有非极性键的晶体是
(填写序号,下同),只存在离子键的是 ,熔化时只破坏
共价键的是 。
(2)下图是XeF4的结构示意图,据此判断XeF4是 (填“极性”、“非极性”)分子。