(1)将饱和的FeCl3溶液逐滴加入到沸水中,溶液的颜色会不断加深,可得到一种红褐色透明液体。写出该过程的离子方程式
在上述溶液中逐滴加入稀硫酸溶液,发生的现象是
反应的离子方程式
(2)有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,则该反应的离子方程式是
其中还原剂与氧化剂的物质的量之比为 。
(18分)(1)请把符合要求的化学方程式的字母填在下列空白处:
①既属于分解反应又是氧化还原反应的是________。
②属于分解反应,但不是氧化还原反应的是________。
③既属于化合反应,又是氧化还原反应的是________。
④属于化合反应,但不是氧化还原反应的是________。
⑤不属于四种基本反应类型的氧化还原反应的是________。
A.(NH4)2SO3 2NH 2NH 3↑+H2O+SO2↑ 3↑+H2O+SO2↑ |
B.2CO+O2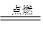 2CO2 2CO2 |
C.2C+SiO2 Si+2CO↑ Si+2CO↑ |
D.NH4NO3 N2O+ 2H2O N2O+ 2H2O |
E.CaCO3 + CO2+ H2O=Ca(HCO3)2
F.MnO2 + 4HCl(浓) MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
(2)根据反应Al+4HNO3(稀)=Al(NO3)3+NO↑+2H2O,回答下列问题:
①还原剂是________,还原产物是________。
②被还原的硝酸与未被还原的硝酸的物质的量比是________。
③用单线桥表示此反应转移的电子数目及方向。
(12分)
现有以下物质:①铝②稀硝酸③氯化氢④氨气⑤甲烷⑥氢氧化钠⑦氯化钙⑧碳酸钡⑨氢氧化铜⑩水 [(1)—(4)用相应物质的序号填写]
(1)可以导电的有
(2)属于电解质的有
(3)属于非电解质的有
(4)属于弱电解质的有
(5)写出⑥和⑧代表物质的电离方程式
某芳香烃A有如下转化关系:
按要求填空:
⑴ 写出反应②和⑤的反应条件:②;⑤.
⑵ 写出A和F结构简式:A;F.
⑶ 写出反应③对应的化学方程式:.
⑷ 属于取代反应的有________________________________(填序号).
⑸ 根据已学知识和获取的信息,以 CH3COOH,
CH3COOH, 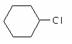 为原料合成重要的化工产品
为原料合成重要的化工产品 。
。
合成路线流程图示例如下:
碳、氢、氧3种元素组成的有机物A,相对分子质量为102,含氢的质量分数为9.8%,分子中氢原子个数为氧原子的5倍。
⑴ 求A的分子式
⑵一定条件下,A与氢气反应生成B,B分子的结构可视为1个碳原子上连接2个甲基和另外2个结构相同的基团。
①A的结构简式是 ,其官能团的名称是
,其官能团的名称是
②A不能发生的反应是(填写序号字母)
a.取代反应b.消去反应c.酯化反应d.还原反应
⑶写出两个与A具有相同官能团、并带有支链的同分异构体的结构简式:
⑷ A还有另一种酯类同分异构体,该异构体在酸性条件下水解,生成两种相对分子质量相同的化合物,其中一种的分子中有2个甲基,此反应的化学方程式是
⑸ 已知环氧氯丙烷可与乙二醇发生如下聚合反应: B也能与环氧氯丙烷发生类似反应生成高聚物,该高聚物的结构简式是
B也能与环氧氯丙烷发生类似反应生成高聚物,该高聚物的结构简式是
为测定某有机化合物A的结构,进行如下实验。
Ⅰ.分子式的确定
(1) 将有机物A置于氧气流中充分燃烧,实验测得:生成5.4gH2O和8.8gCO2,消耗氧气6.72L(标准状况下)。则该物质分子中碳、氢、氧原子个数比为
(2) 质谱仪测定有机物A的相对分子质量为46,则该物质的分子式是
(3) 根据价键理论,预测 A的可能结构并写出结构简式
A的可能结构并写出结构简式
Ⅱ.结构式 的确定
的确定
(4) 核磁共振氢原子光谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。
例如:甲基氯甲基醚(Cl—CH2—O—CH3)有两种氢原子(图1)。经测定,有机物A的核磁共振氢谱示意图(图2),则A的结构简式为。
Ⅲ.性质实验
(5) A在一定条件下脱水可生成B,B可合成包装塑料C。体育比赛中当运动员肌肉扭伤时,队医随即用氯乙烷(沸点为12.27℃)对受伤部位进行局部冷冻麻醉。请用B选择合适的方法制备氯乙烷,要求原子利用率为100%,请写出制备反应方程式
为: