某学习小组按右图在实验室制取氨气并探究铜的有关性质(部分夹持仪器未画出)。请回答: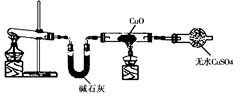
(1)制取氨气的化学方程式是 。
(2)① 实验现象为:黑色CuO变为红色(生成单质a);白色无水CuSO4粉末变为蓝色; 同时生成一种无色气体,该气体无污染。请写出氨气与CuO反应的化学方程式 。
②碱石灰的作用是 。
(3)将上述生成的单质a在热水浴中进行4个实验,部分实验报告如下表所示。
| 序号 |
实验操作 |
实验现象 |
| Ⅰ |
稀硫酸中加入该单质a |
无明显变化 |
| Ⅱ |
硝酸钠溶液中加入该单质a |
无明显变化 |
| Ⅲ |
硫酸钠溶液中加入该单质a |
无明显变化 |
| Ⅳ |
稀硫酸中加入硝酸钠溶液 |
无明显变化 |
| 再加入该单质a |
有无色气泡;溶液变蓝 |
①实验I、II、III的目的是 。
②实验Ⅳ中反应的本质是(用离子方程式表示) 。
测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数及物质的量分数。现有下列实验用品:中学化学实验常用仪器、1000 mL烧杯、100 mL量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19 g·cm-3)、水。按图示装置进行实验,回答下列问题。(设合金样品完全反应,产生的气体体积不超过100 mL)
(1).补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
①将称量后的合金样品用铜网小心包裹好,放在1000 mL烧杯底部,把短颈漏斗倒扣在样品上面。
②_________________________________________________________________________。
③_________________________________________________________________________。
④_________________________________________________________________________。
(2)合金样品用铜网包裹的目的是什么?
________________________________________________________________________。
(3).已知一定质量的铝锌合金的总物质的量为n,实验测得的气体体积为V1mL(已经换算为标准状况)。则铝锌合金中铝的物质的量分数为:_________________。(用含n和V1的式子表示)
(4)本装置也可用于测定金属锌(或其它金属)的相对原子质量,若m g金属锌进行实验,测得的气体体积为V2mL(已经换算为标准状况)。则金属锌的相对原子质量为:_________________。(用含m和V2的式子表示)
聚合硫酸铁又称聚铁,化学式为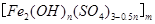 ,广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O )过程如下:
,广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O )过程如下:
(1)验证固体W焙烧后产生的气体含有SO2的方法是___。
(2)制备绿矾时,向溶液X中加入过量___,充分反应后,经_____操作得到溶液Y,再经浓缩,结晶等步骤得到绿矾。
(3)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH的操作方法为____。若溶液Z的pH偏小,将导致聚铁中铁的质量分数偏_____。
(4)古代将绿矾煅烧可制绿矾油(也叫镪水,即硫酸)和红色颜料(Fe2O3),请写出有关的化学方程式:。
(5)绿矾还可用以下方法生产红色颜料(Fe2O3),其具体操作流程是:将5560kg绿矾(摩尔质量为278 g/mol)溶于水中,加入适量氢氧化钠溶液恰好完全反应,鼓入足量空气搅拌,产生红褐色胶体;再向红褐色胶体中加入16680 kg 绿矾和560 kg铁粉,鼓入足量空气搅拌,反应完成后,有大量Fe2O3附着在胶体粒子上以沉淀形式析出;过滤后,沉淀经高温灼烧得红色颜料。若所得滤液中溶质只有硫酸钠和硫酸铁,则理论上可生产红色颜料____________________kg。
谷氨酸一钠盐是味精的主要成分,谷氨酸一钠盐在水溶液中存在如下平衡: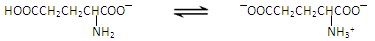
(1)当前我国生产味精主要采用淀粉发酵法,其中第一步是使淀粉水解为单糖。实验室中检验淀粉水解产物可选用的试剂是。
| A.NaOH溶液、氨水、AgNO3溶液 | B.H2SO4溶液、氨水、AgNO3溶液 |
| C.NaOH溶液、CuSO4溶液 | D.H2SO4溶液、CuSO4溶液 |
(2)“沙伦逊甲醛滴定法”可用于测定味精中谷氨酸一钠盐的含量。其方法如下:
将一定质量的味精样品溶于水,再向溶液中加入36%甲醛溶液,发生的反应如下:
R—NH2+HCHO→R—N=CH2+H2O(R表示除“-NH2”外的基团),再以酚酞为指示剂,用NaOH溶液进行滴定。
①上述测定过程中加入甲醛的目的是。
②滴定终点的实验现象为。
(3)味精中常含食盐,有两个同学分别设计甲、乙两种方案来测定味精中NaCl的含量。
①甲方案:取一定质量味精样品溶于水,加入足量稀硝酸酸化的硝酸银溶液,充分反应后,(填写操作步骤),称量沉淀质量。
②乙方案:取mg味精溶于水,加入过量浓度为c1mol·L—1的AgNO3溶液,再加入少量溶液做指示剂,用浓度为c2mol·L—1的NH4SCN溶液进行滴定,当溶液变为红色时,达到滴定终点。已知:AgSCN是难溶于水的沉淀。
设测定过程中所消耗的AgNO3溶液和NH4SCN溶液的体积分别为V1mL和V2mL,则该味精样品中NaCl的质量分数是。
(15分)碱式碳酸铜的成分有多种,其化学式一般可表示为xCu(OH)2·yCuCO3。
(1)孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2·CuCO3。某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
实验1:将2.0mL 0.50 mol·L—1的Cu(NO3)2溶液、2.0mL 0.50 mol·L—1的NaOH溶液和0.25 mol·L—1的Na2CO3溶液按表Ⅰ所示体积混合。
实验2:将合适比例的混合物在表Ⅱ所示温度下反应。
实验记录如下:
| 编号 |
V (Na2CO3)/ mL |
沉淀情况 |
编号 |
反应温度/℃ |
沉淀情况 |
|
| 1 |
2.8 |
多、蓝色 |
1 |
40 |
多、蓝色 |
|
| 2 |
2.4 |
多、蓝色 |
2 |
60 |
少、浅绿色 |
|
| 3 |
2.0 |
较多、绿色 |
3 |
75 |
较多、绿色 |
|
| 4 |
1.6 |
较少、绿色 |
4 |
80 |
较多、绿色(少量褐色) |
表Ⅰ表Ⅱ
①实验室制取少许孔雀石,应该采用的条件是。
②80℃时,所制得的孔雀石有少量褐色物质的原因是。
(2)实验小组为测定上述某条件下所制得的碱式碳酸铜样品组成,利用下图所示的装置(夹持仪器省略)进行实验:
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中。
步骤2:打开活塞K,鼓入空气,一段时间后关闭,称量相关装置的质量。
步骤3:加热装置B直至装置C中无气泡产生。
步骤4:。
步骤5:称量相关装置的质量。
①装置A的作用是;若无装置E,则实验测定的x/y的值将(选填“偏大”、“偏小”或“无影响”)。
②某同学在实验过程中采集了如下数据:
A.反应前玻璃管与样品的质量163.8g
B.反应后玻璃管中残留固体质量56.0g
C.装置C实验后增重9.0g
D.装置D实验后增重8.8g
为测定x/y的值,你认为可以选用上述所采集数据中的(写出所有组合的字母代号)一组即可进行计算,并根据你的计算结果,写出该样品组成的化学式。
(12分)酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式。SnSO4是一种重要的硫酸盐,广泛应用于镀锡工业,其制备路线如下: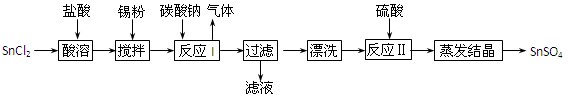
回答下列问题:
(1)SnCl2用盐酸而不用水直接溶解的原因是,加入Sn粉的作用是。
(2)反应I生成的沉淀为SnO,写出该反应的化学方程式:。
(3)检验沉淀已经“漂洗”干净的方法:。
(4)反应Ⅱ硫酸的作用之一是控制溶液的pH,若溶液中c(Sn2+)=1.0mol·L—1,则应控制溶液pH。已知:Ksp[Sn(OH)2]=1.0×10—26。
(5)酸性条件下,SnSO4还可以用作双氧水去除剂,试写出发生反应的离子方程式:。