已知水在25 ℃和95 ℃时,其电离平衡曲线如右图所示: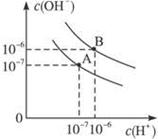
⑴则25 ℃时水的电离平衡曲线应为 ___ (填“A”或“B”),请说明理由 ________________ 。
⑵95 ℃时PH=2的NaOH溶液中由水电离的c(H+) ______。
⑶25 ℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为 _________ 。
⑷25 ℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 _____ 。
⑸曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。请分析原因: 。
⑹95 ℃时,某氨水与氯化铵的混合溶液的PH=7,则c(NH4+)______c(Cl-)(填“>”、“<”、或“=”)
(8分)分析氧化还原反应并填空WO3+H2 W+3H2O
W+3H2O
氧化剂_____________,还原剂________ 氧化产物________,还原产物__________
化学科学在药物的开发、合成和使用中起着至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可治疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
____________________________________________________。
(2)现有一瓶胃舒平药片(复方氢氧化铝),写出其中和胃酸的作用原理(离子方程式)____________________________________________________
(3)检验Fe3+常用的试剂除碱外,还可以用_____________(填化学式),现象是_____________。
(1)除去亚铁离子中混有的铁离子用试剂______,离子方程式_______________________
(2)除去混在氯化钠(NaCl)中的少量氯化镁(MgCl2), 用_____________(试剂),离子方程式是___________________________
由等物质的量烃A和烃的衍生物B组成的混合物共0.5摩,恰好能和1.25摩O2完全燃烧生成1molCO2和1molH2O,请用分子式给出A和B的可能组合方式(可不填满)
| A |
B |
|
| (1) |
||
| (2) |
||
| (3) |
||
| (4) |
||
| (5) |
(12分)某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图。加热聚丙烯废塑料得到的产物如下表:
| 产物 |
氢气 |
甲烷 |
乙烯 |
丙烯 |
苯 |
甲苯 |
碳 |
| 质量分数(%) |
12 |
24 |
12 |
16 |
20 |
10 |
6 |
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
写出反应②③的化学方程式:____________________、____________________。
(2)试管B收集到的产品中,能使高锰酸钾酸性溶液褪色的物质,其一氯代物有_____种。
(3)锥形瓶C中观察到的现象______________。
(4)写出C中逸出的气体在工业上的两种用途:________________、_______________。