设阿伏加德常数为NA。则下列说法正确的是
| A.常温常压下,11.2L甲烷中含有的氢原子数为2NA |
| B.标准状况下,0.3mol二氧化硫中含有氧原子数为0.3NA |
| C.常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA |
| D.常温下,1L 0.1mol/L MgCl2溶液中含Mg2+数为0.2NA |
下列描述中,不符合生产实际的是
| A.电解熔融的氧化铝制取金属铝,用铁作阳极 |
| B.电解法精炼粗铜,用纯铜作阴极 |
| C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 |
| D.在镀件上电镀锌,用锌作阳极 |
市场上常用的一种锂离子电池的电池反应式为:LiC6+2Li0.35NiO2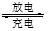 2Li0.85NiO2+C6,下列说法中不正确的是
2Li0.85NiO2+C6,下列说法中不正确的是
| A.该电池不能用水溶液作为电解质 |
| B.放电时,Li+向负极移动 |
| C.充电时,电极Li0.85NiO2质量会减小 |
| D.放电时,负极的反应为:LiC6-e-=Li++C6 |
下列叙述I和II均正确且有因果关系的是
| 选项 |
叙述I |
叙述II |
| A |
铜丝深入稀硝酸溶液中,溶液变蓝 |
铜丝与硝酸发生了置换反应 |
| B |
浓硫酸具有吸水性和强氧化性 |
把浓硫酸滴到蔗糖表面,蔗糖变黑膨胀 |
| C |
Fe3+具有氧化性 |
FeCl3溶液用于回收废旧电路板中的Cu |
| D |
BaSO4难溶于酸 |
向某溶液加入Ba(NO3)2溶液,再加入足量稀HCl,得到白色沉淀,则原溶液含SO42- |
下列关于实验现象的描述不正确的是
| A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B.用锌片做阳极,铁片做做阴极,电解氯化锌溶液,铁片表面出现一层锌 |
| C.把要保护的金属与直流电负极相连,这种方法叫牺牲阳极的阴极保护法 |
| D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
下列叙述I和II均正确且有因果关系的是
| 选项 |
叙述I |
叙述II |
| A |
SO2具有漂白性 |
SO2可使溴水褪色 |
| B |
非金属性:F>Cl |
酸性:HF>HCl |
| C |
Si是半导体 |
Si用于制造光导纤维 |
| D |
35Cl和37Cl互为同位素 |
35Cl和37Cl化学性质几乎相同 |