2g Cu2S和CuS的混合物在酸性溶液中用400mL 0.075mol/L KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350mL 0.1mol/L(NH4)2Fe(SO4)2溶液完全反应。
(1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
MnO4-+ Fe2++ H+= Mn2++ Fe3++H2O
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为 mol。
(3)欲配制500mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为 g。
(4)混合物中Cu2S的质量分数为 。
具有水果香味的中性物质A可以发生下列变化:
(1) 推断下述物质的结构简式:
A:________________ B: ________________
C: ________________ D: ________________
(2) 写出下列变化的化学方程式,并注明化学反应类型:
A+NaOH→B+C:___________________________反应类型____________
C→G:____________________________________反应类型____________
G→高分子化合物:反应类型
今有三种化合物结构如下: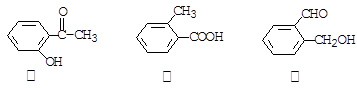
(1) 请写出丙中含氧官能团的名称:。
(2) 请判断上述哪些化合物互为同分异构体:___。
(3)写出化合物乙与小苏打溶液反应的化学方程式:
某烯烃,经与氢气加成反应可得到结构简式为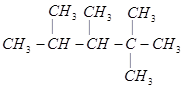 、的烷烃,则此烯烃可能的结构简式是:___________、___________、___________。
、的烷烃,则此烯烃可能的结构简式是:___________、___________、___________。
目前世界上60%的镁是从海水提取的。海水提镁的主要流程如下: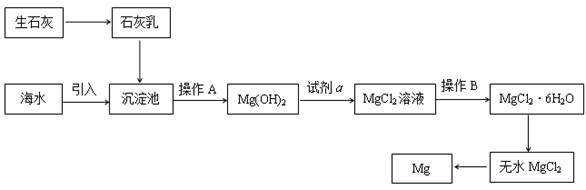
请回答下列问题:
(1)从离子反应的角度思考,在海水中加入石灰乳的作用是 ,写出在沉淀池的离子方程式 。
(2)石灰乳是生石灰与水形成的化合物,从充分利用海洋化学资源,提高经济效益的角度,生产生石灰的主要原料来源于海洋中的 。
(3)操作A是 , 操作B是 。
(4)加入的足量试剂a是 (填化学式)。
(5)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
。从考虑成本和废物循环利用的角度,副产物氯气可以用于 。
(6)海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?
。
(7)有同学认为:可直接加热Mg(OH)2得到MgO,再电解熔融MgO制金属镁,这样可简化实验步骤,体现实验的简约性原则。你 (填“同意”或“不同意”)该同学的想法,理由是 。
已知A是一种分子量为28的气态烃,能发生以下转化: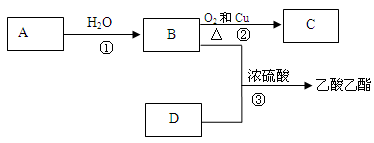
(1)写出B、D化合物中官能团:
B中含官能团(写名称);
D中含官能团(写结构简式);
(2)写出反应的化学方程式
①反应类型:
② 反应类型:
③ 反应类型:_________