盛有NO 和 NO2的混合气体的量筒倒立在盛有水的水槽中,过一段时间后,量筒内的气体体积减小为原来的一半 。则原混合气体中NO 和 NO2的体积比是 ( )
| A.3∶1 | B.1∶3 | C.2∶1 | D.1∶2 |
道尔顿的原子学说曾经对世界化学的发展起了很大的作用。他的学说中,包含有下述三个论点:①原子是不能再分的粒子;②同种元素的原子的各种性质和质量都相同;③原子是微小的实心球体。从现代的观点看,你认为错误的有( )
| A.只有① | B.只有② | C.只有③ | D.①②③ |
同温同压下,等容积的两个密闭容器中分别充满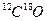 和
和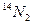 两种气体,以下关于这两个容器中气体的说法正确的是( )
两种气体,以下关于这两个容器中气体的说法正确的是( )
| A.质子数相等,质量不相等 |
| B.原子数相等,质量不相等 |
| C.分子数、质量分别相等 |
| D.分子数、中子数和质子数都分别相等 |
核内中子数为N的R2+,质量数为A,则ng它的氧化物中所含质子的物质的量为( )
A.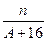 (A-N+8) mol (A-N+8) mol |
B.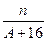 (A-N+10) mol (A-N+10) mol |
| C.(A-N+2) mol |
D. (A-N+6) mol (A-N+6) mol |
某粒子用符号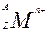 表示,下列关于该粒子的叙述正确的是( )
表示,下列关于该粒子的叙述正确的是( )
| A.所含质子数为(A-n) |
| B.所含中子数为(A-Z) |
| C.所含电子数为(Z+n) |
| D.中子数-电子数=A-2Z+n |
 (核磁共振)可以用于含碳化合物的结构分析。
(核磁共振)可以用于含碳化合物的结构分析。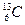 表示的碳原子( )
表示的碳原子( )
| A.核外有13个电子 |
| B.质量数为13,核电荷数为6,质子数为7 |
| C.核内有6个质子,核外有7个电子 |
| D.质量数为13,核内有6个质子,7个中子 |