选择下列实验方法分离物质,将分离方法的序号填在横线上。
A萃取分液法 B加热分解法 C结晶法
D分液法 E蒸馏法 F过滤法
⑴ 分离饱和食盐水与沙子的混合物。
⑵ 从硝酸钾和氯化钠的混合溶液中获得硝酸钾。
⑶ 分离水和汽油的混合物。
⑷ 从溴的水溶液里提取溴。
水垢可以看作由多种物质组成的混合物,为研究含有 、
、 、
、 的水所形成水垢的化学组成,取干燥的水垢6.32g,加热使其失去结晶水,得到5.78g剩余固体A;高温灼烧A至恒重,残余固体为CaO和MgO,放出的气体用过量的Ba(OH)2溶液吸收,得到11.829沉淀。
的水所形成水垢的化学组成,取干燥的水垢6.32g,加热使其失去结晶水,得到5.78g剩余固体A;高温灼烧A至恒重,残余固体为CaO和MgO,放出的气体用过量的Ba(OH)2溶液吸收,得到11.829沉淀。
(1)通过计算确定A中是否含有MgCO3。
(2)5.78g剩余固体A灼烧至恒重时当生成的气体完全被碱石灰吸收,碱石灰增重2.82g,通过计算确定A中各成分的物质的量,并计算水垢中的碳酸盐的质量分数.
(1)图所示装置为化学实验中常见的仪器,它除了用于洗气外,还有其他用途。
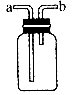

①医院给病人输氧时往往在氧气罐与病人呼吸器之间安装盛水的该装置,通过观察气泡产生情况以便调节供氧速率,此时氧气从口导入。
②实验室用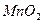 和浓HCl制
和浓HCl制 实验中,将生成的
实验中,将生成的 通入NaOH溶液之前,先将
通入NaOH溶液之前,先将 从该装置管进,从管导出,此时该装置起的作用是防止NaOH倒流。
从该装置管进,从管导出,此时该装置起的作用是防止NaOH倒流。
③当用此装置收集NO时,需采取什么措施?
(2)被称为“魔棒”的荧光棒已成为节日之夜青少年的喜爱之物,其发光原理是利用过氧化氢氧化草酸酯产生能量,该能量被传递给荧光物质后便发出荧光。回答下列问题:
①有人说,发光的魔棒不能凑近石油气之类的可燃性气体,否则会导致爆炸,是否正确?说明理由。
②通过挤压,使过氧化氢与革酸酯混合反应,导致魔棒发光,一段时间后,光的亮度降低,此时,把魔棒往手心上敲打几下,亮度会重新增大,原因是什么?(提示:草酸酯是一种有较高黏度的有机化合物)
③在设计魔棒时,其连续发光的能力在8~12h,如果在发光中途,把它放人冰箱的冷冻室中,发光便会停止或基本停止。把魔棒从冷冻室中取出静止一会儿,它又会连续发光,原因是什么?
下列各单质与化合物之间的关系如下图,单质及化合物的组成元素皆为短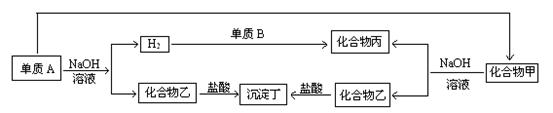
周期元素,请回答:
(1)若沉淀丁不溶于过量的盐酸,甲为 ;乙为 。
若沉淀丁能溶于过量的盐酸,丁为 。
(2)单质B一定是__________。写出丙的电子式: 。
(3)写出有关反应方程式
①沉淀丁不溶于过量盐酸时,写出A+NaOH的反应:
②沉淀丁能溶于过量盐酸时,写出化合物乙与过量盐酸反应的方程式:
有一工业烧碱(含氯化钠),现要求采用学过的定量实验的方法测定此工业烧碱中氢氧化钠的质量分数(假设各步实验中试样的损失忽略不计),请完成如下实验报告。
实验报告
(一)实验目的:工业烧碱中氢氧化钠的质量分数测定
(二)实验原理:(写出有关离子反应方程式):_____________________________,
(三)实验试剂:工业烧碱、标准浓度的盐酸、甲基橙。
(四)实验仪器:铁架台(成套)、天平、烧杯、锥形瓶、移液管、胶头滴管、100ml量筒、 ________、_______。
(五)按实验顺序填写实验步骤:(中和滴定法)
______、溶解、移液管量取一定体积的待测液于洁净的锥形瓶中、__________、用标准盐酸滴定至终点。
当滴定至溶液由______色变为_____色,且半分钟不腿色时停止滴定。在相同条件下重复二次。
(六)数据处理及问题讨论:
1、若要测定样品中氢氧化钠的质量分数,实验中至少需要测定那些实验数据?_______________________________________。
2、取a克样品,配置100mL溶液,取20mL待测液,用C mol/L的标准盐酸滴定至终点,消耗盐酸VmL。试写出样品中氢氧化钠的质量分数表达式为: 。
反应aA(g) +bB(g)cC(g)+d D(g)在容积不变的密闭容器中达到平衡,且起始时A与B的物质的量之比为a∶b。则
(1)平衡时A与B的转化率之比是 。
(2)若同等倍数地增大A、B的物质的量浓度,要使A与B的转化率同时增大,(a+b)与(c+d)所满足的关系是(a+b) (c+d ) (填“>”“=”“<”或“没关系”)。
(3)设定a="2" ,b=1,c=3,d=2,在甲、乙、丙、丁4个相同的容器中A的物质的量依次是2 mol、1 mol、2 mol、1 mol,B的物质的量依次是1 mol、1 mol、2 mol、2 mol,C和D的物质的量均为0。则在相同温度下达到平衡时,A的转化率最大的容器是 ,B的转化率由大到小的顺序是 (填容器序号)。