有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法正确的是( )
①每消耗1molCH4可以向外电路提供8mole-
②负极上CH4失去电子,电极反应式CH4+10OH--8e-=CO32-+7H2O
③负极上是O2获得电子,电极反应式为 O2+2H2O+4e-=4OH-
④电池放电后,溶液pH不断升高
| A.①② | B.①③ | C.①④ | D.③④ |
灰锡结构松散,不能用于制造器皿,而白锡结构坚固,可以制造器皿。现把白锡制成的器皿放在0 ℃、100 kPa的室内存放,它会不会变成灰锡而不能再继续使用(已知在0 ℃、100 kPa条件下白锡转化为灰锡反应的焓变和熵变分别为ΔH=-2 180.9 J·mol-1,ΔS=-6.6 J·mol-1·K-1当ΔH-TΔS<0时能自发反应)
| A.会变 | B.不会变 |
| C.不能确定 | D.升高温度才会变 |
向某密闭容器中充入1 mol CO 和2 mol H2O(g),发生反应:CO+H2O(g) CO2+H2.当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是
CO2+H2.当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是
| A.0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2 |
| B.1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2 |
| C.0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2 |
| D.0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2 |
在一个固定体积的密闭容器中,加入2 mol A和1 mol B发生反应:2A(g)+B(g) 3C(g)+D(g),达到平衡时C的浓度为W mol·L-1。若维持容器体积和温度不变,按下列四种方法改变起始物质及其量,达到平衡后C的浓度仍为W mol·L-1的是
3C(g)+D(g),达到平衡时C的浓度为W mol·L-1。若维持容器体积和温度不变,按下列四种方法改变起始物质及其量,达到平衡后C的浓度仍为W mol·L-1的是
| A.4 mol A+2 mol B | B.2 mol A+1 mol B+3 mol C+1 mol D |
| C.3 mol C+1 mol D+1 mol B | D.3 mol C+1 mol D |
一定温度下,在2 L的密闭容器中发生如下反应:A(s)+2B(g)  2C(g) ΔH<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2.下列有关说法正确的是
2C(g) ΔH<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2.下列有关说法正确的是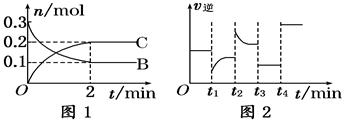
A.反应开始2 min内,v(B)=0.1 mol/(L·min)
B.t1时改变的条件可能是升高温度
C.t3时改变的条件可能是加压,此时c(B)不变
D.t4时可能是使用了催化剂,此时c(B)不变
如图是恒温下某化学反应的反应速率随反应时间变化的示意图.下列叙述与示意图不相符合的是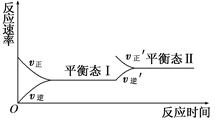
| A.反应达平衡时,正反应速率和逆反应速率相等 |
| B.该反应达到平衡态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡态Ⅱ |
| C.该反应达到平衡态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ |
| D.同一种反应物在平衡态Ⅰ和平衡态Ⅱ时浓度不相等 |