下表是元素周期表中的一部分,回答下列有关问题:
| 族 周期 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
| 2 |
|
|
|
⒀ |
⑴ |
|
|
|
| 3 |
⑶ |
⑸ |
|
|
⑺ |
⑻ |
|
|
| 4 |
⑽ |
⑾ |
|
|
|
|
|
(1)⑺⑻⑽⑾四种元素形成的离子,半径由大到小的顺序是
(填元素符号或化学式,下同)。
(2)元素⑻的单质与水反应的离子方程式为 ;元素⑶的单质与水反应的离子方程式为 。
(3)⑶的最高价氧化物对应水化物与⑸的氧化物相互反应的离子方程式 。
(4)元素⑴的单质的结构式为 ,元素⒀最高价氧化物的电子式 。
A、B、C、D、E五种元素为1~18号元素。已知:它们的原子序数依次增大,A、B两种元素的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多2;C元素原子的电子层数及最外层电子数都比E元素的少1;D和E的原子序数之和为30。它们两两形成的化合物有甲、乙、丙、丁四种。这四种化合物中原子个数比如下表:
| 甲 |
乙 |
丙 |
丁 |
|
| 化合物中各元素原子个数比 |
A和C 1∶1 |
B和A 1∶2 |
D和E 1∶3 |
B和E 1∶4 |
(1)写出元素符号:A__________,B__________,C__________,D__________,E__________。
(2)向甲的水溶液中加入MnO2,氧化产物是____________________。
(3)已知有机物乙的分子为平面结构,键角都为120°,实验室制取乙的化学方程式为____________________。
(4)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会产生大量的气体和难溶物,有关离子方程式是____________________。
(5)写出E原子的电子排布式____________________。
在A、B、C、D四种元素中,A为地壳中含量最多的元素;B的单质在所有气体中密度最小;C元素的原子失去两个电子后,其电子层结构和氩原子相同;D元素的原子核外有三个能层,各能层电子数之比为1∶4∶1。
(1)写出上述四种元素的名称:A__________,B__________,C__________,D__________。
(2)写出C2+的电子排布式__________。
(3)指出A、B、C三种元素所形成化合物中包含化学键类型____________________。
(4)分别用电子式表示:A与B形成化合物B2A、A与C形成化合物CA的过程。
一般较强酸可制取较弱酸, 这是复分解反应的规律之一。已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH: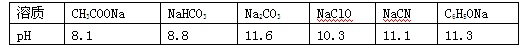
(1) 请根据上述信息判断下列反应不能发生的是________(填编号)。
| A.CH3COOH+NaCN===CH3COONa+HCN |
| B.CO2+H2O+2NaClO===Na2CO3+2HClO |
| C.2HCN+Na2CO3―→2NaCN+CO2+H2O |
| D.Na2CO3+C6H5OH―→NaHCO3+C6H5ONa |
E.CO2+H2O+C6H5ONa―→NaHCO3+C6H5OH
(2)己知常温时Ksp(AgCl)=1.8×10-10 mol2.L-2,向50 mL 0.018 mo1.L-l的AgNO3溶液中加入相同体积0.020 mol.L-1的盐酸,则c(Ag+)=。
物质(t-BuNO)2在正庚烷溶剂中发生如下反应:(t-BuNO)2 2(t-BuNO) 。
2(t-BuNO) 。
(1)当(t-BuNO)2的起始浓度(c0)为0.50 mol·L-1时,实验测得20℃时的平衡转化率(α)是65 %。列式计算20℃时上述反应的平衡常数K =。
(2)一定温度下,随着(t-BuNO)2的起始浓度增大,其平衡转化率 (填“增大”、“不变”或“减小”)。
(3)实验测得该反应的ΔH =" +" 50.5 kJ·mol-1,活化能Ea = 90.4 kJ·mol-1。下列能量关系图合理的是。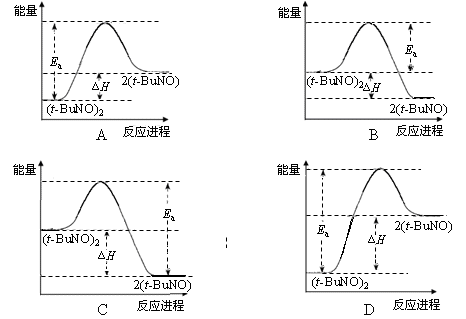
(4)结合ΔS推测该反应的在(填“较高”或“较低”)温度下有利于该反应自发进行。
(共12分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
Ⅰ.目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3.25 mol H2,在一定条件下发生反应,测定CO2、CH3OH(g)和H2O(g)的浓度随时间变化如下图所示: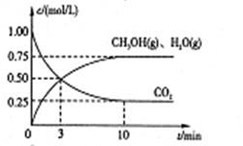
(1)从反应开始到平衡,氢气的平均反应速率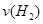 =mol/(L·min)
=mol/(L·min)
(2)该条件下CO2的转化率为。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是。
| A.升高温度 | B.恒容时充入氮气 |
| C.将水蒸气从体系中分离 | D.用更有效的催化剂 |
Ⅱ.下图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题: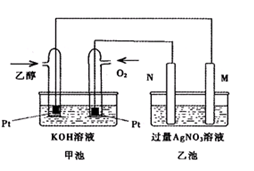
(1)M极的电极材料为 。
(2)加入乙醇的铂电极的电极反应式为。
(3)在此过程中乙池中某一电极析出金属银4.32g时,此时乙池溶液的体积为400mL,则乙池中溶液的pH为。
(4)若在常温常压下,1g C2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,表示该反应的热化学方程式为。