已知水在25℃和95℃时,其电离平衡曲线如右图所示: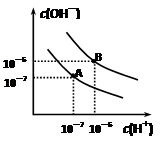
⑴则25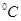 时水的电离平衡曲线应为 (填“A”或“B”)。
时水的电离平衡曲线应为 (填“A”或“B”)。
⑵25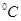 时,将
时,将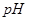 =8的NaOH溶液与
=8的NaOH溶液与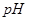 =5的
=5的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的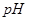 =7,则NaOH溶液与
=7,则NaOH溶液与 溶液的体积比为 。
溶液的体积比为 。
⑶95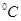 时,0.1 mol/L的NaOH溶液的pH值是 。
时,0.1 mol/L的NaOH溶液的pH值是 。
⑷95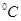 时,若100体积
时,若100体积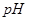 1=
1=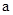 的某强酸溶液与1体积
的某强酸溶液与1体积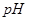 2=b的某强碱溶液混合后溶液呈中性,则混合前,
2=b的某强碱溶液混合后溶液呈中性,则混合前,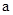 与b之间应满足的关系是
与b之间应满足的关系是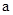 = (用含b的代数式表示),a+b_______14(填“<”、“=”或“>”)。
= (用含b的代数式表示),a+b_______14(填“<”、“=”或“>”)。
聚甲基丙烯酸酯纤维具有质轻、频率宽等特性,广泛应用于制作光导纤维。已知A为某种聚甲基丙烯酸酯纤维的单体,其转化关系如下: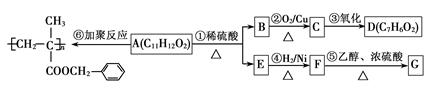
(1)D含有的含氧官能团的名称是______________。
(2)⑤的反应类型是____________。
(3)根据系统命名法,F的名称是______ _______。
_______。
(4)E不能发生的反应是(填写字母标号)
| A.能使酸性高锰酸钾溶液褪色 | B.能使溴的CCl4溶液褪色 |
| C.一定条件下,能够发生消去反应 | D.一定条件下,能够发生取代反应 |
(5)F的同分异构体中,属于酯类的有____________种。
(6)G的结构简式为。
(7)一定条件下,E可以发生加聚反应,化学方程式为。
空气质量高低直接影响着人类的生产和生活,它越来越受到人们的关注。被污染的空气中杂质的成分有多种,其中计入《空气质量日报》空气污染指数的项目有SO2、CO、NO2、O3和可吸入颗粒物等。
请回答下列问题:
(1)S、N、O的的第一电离能由大到小的顺序为。
(2)SO2、CO、NO2、O3常温下均为气体,固态时均属于晶体。
(3)随着人们生活质量的提高,室内的环境安全和食品安全越来越为人们所关注。甲醛(HCHO)是室内主要空气污染物之一(其沸点是–19.5 ℃),甲醇(CH3OH)是“假酒”中的主要有害物质(其沸点是64.65 ℃)。甲醛分子中C原子采取杂化轨道方式。甲醇的沸点明显高于甲醛的主要原因是:__________。
(4)CuCl的盐酸溶液能够与CO发生反应:CuCl+CO+H2O=Cu(CO)Cl·H2O,该反应可用于测定空气中CO含量。
①写出铜原子的基态电子排布式。
②CuCl的晶体结构如下图甲所示,与同一个Cl-距离最近的相邻Cu+有个。
③Cu(CO)Cl·H2O的结构如上图乙所示,图中标示出8个是共价键,其中6个是配位键,请在图中用箭头标示出。
金属钛被称为铁和铝之后崛起的“第三金属”,常见化合价为+4。它是空间技术、航海、化工、医疗上不可缺少的材料。
Ⅰ.工业上用钛铁矿(主要成分FeTiO3)制备金属钛的一种工艺流程如下图(部分产物略去):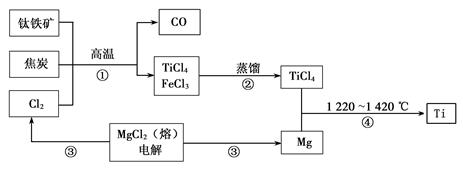
(1)步骤①反应的化学方程式为:2FeTiO3 + 6C + 7Cl2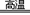 2FeCl3 + 2TiCl4 + 6CO,还原剂是。
2FeCl3 + 2TiCl4 + 6CO,还原剂是。
(2)步骤②分离出TiCl4的方法,利用了TiCl4与FeCl3的不同。
(3)步骤④反应的化学方程式为________________________________,该反应在氩气中进行的理由是______________________________。
(4)绿色化学提倡物料循环。以上流程中,可用于循环的物质除Cl2、Mg外,还有____________。
II. 工业上也可用TiO2通过下述两种方法制备金属钛:
方法一:先将TiO2氯化为TiCl4,再还原得到Ti。
(5)氯化反应TiO2 (s ) +2Cl2 (g)
) +2Cl2 (g)  TiCl4(l) + O2 (g)无法自发正向进行,在反应器中加入碳,则在高温条件下反应可顺利进行。试从化学平衡角度解释,往氯化反应器中加碳的原因:。
TiCl4(l) + O2 (g)无法自发正向进行,在反应器中加入碳,则在高温条件下反应可顺利进行。试从化学平衡角度解释,往氯化反应器中加碳的原因:。
方法二:以熔融盐为电解液电解TiO2获得Ti。其中,碳块为阳极,电极反应式为:2O2ˉ– 4eˉ=O2↑;TiO2作阴极,被还原。
(6)阴极的电极反应式为。
(7)电解过程中需定期向电解槽中加入碳块的原因是。
A、D、E、X、Y是原子序数依次增大的短周期主族元素。其中X原子最外层电子数是内层电子总数的3倍;X、Y同族;A与X、Y既不同族也不同周期;D元素的某种同位素原子在考古方面有重要应用。
(1)Y的离子结构示意图为。
(2)钠、A和X三种元素组成的化合物,其所含的化学键类型有。
(3)甲由A、E两种元素组成,分子中含有18个电子,只存在共价单键。常温下甲是一种无色液体。
①甲是一种二元弱碱, 写出其一级电离方程式:。
写出其一级电离方程式:。
②甲在碱性溶液中能够将CuO还原为Cu2O, 已知每1mol甲参加反应有 4 mol电子转移,该反应的化学方程式为:。
已知每1mol甲参加反应有 4 mol电子转移,该反应的化学方程式为:。
(4)处理含DX、YX2烟道气污染的一种方法,是在催化剂作用下使两者反应,产物之一为单质Y。已知反应生成1 g Y固体单质时放出8.4 kJ热量,此反应的热化学方程式为。
(5)将0.050 mol YX2(g)和0.030 mol X2(g)放入容积为1 L的密闭容器中,反应: X2(g) +2YX 2(g) 2YX3(g)在一定条件下达到平衡。
2YX3(g)在一定条件下达到平衡。
①若其他条件不变,增大体系的压强,平衡常数K(填“增大”、“减小”或“不变”)。
②平衡时测得c(X2)=0.010 mol·Lˉ1。该条件下反应的平衡常数K=,YX2的平衡转化率为。
某芳香化合物H常用作食 用香精。用质谱法测得其相对分子质量为162,分子中C、H、O原子个数比为5 :5 :1。H只有一个支链;它能与溴的四氯化碳溶液发生加成反应。且在碱性条件下能发生水解反应,产物之一是甲醇。G是H的同分异构体。用芳香烃A为原料合成G的路线如下:
用香精。用质谱法测得其相对分子质量为162,分子中C、H、O原子个数比为5 :5 :1。H只有一个支链;它能与溴的四氯化碳溶液发生加成反应。且在碱性条件下能发生水解反应,产物之一是甲醇。G是H的同分异构体。用芳香烃A为原料合成G的路线如下: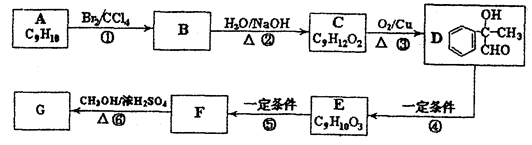
(1)G的分子式是____________,H的结构简式是_________________。
(2)化合物C的官能团名称是________________,反应②、⑤的反应类型分别是______________、______________。预测E分子中苯环侧链核磁共振氢谱峰面积(由小到大)之比为________________。
(3)写出反应①、⑥的 化学方程式:
化学方程式:
①___________________________________________________;
⑥___________________________________________________,
(4)符合下列条件的F的同分异构体的结构简式是_______________________。
a.分子内含苯环,且苯环上只有一个支链;
b.在一定条件下,1mol该物质与足量银氨溶液充分反应,生成4mol银单质。