已知下列热化学方程式:
Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol
Fe2O3(s)+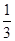 CO(g)===
CO(g)===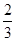 Fe3O4(s)+
Fe3O4(s)+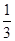 CO2(g) ΔH=-15.73 kJ/mol
CO2(g) ΔH=-15.73 kJ/mol
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH=+640.4 kJ/mol
则14 g CO气体还原足量FeO固体得到Fe单质和CO2气体时对应的ΔH约为( )
| A.-218 kJ/mol | B.-109 kJ/mol | C.+218 kJ/mol | D.+109 kJ/mol |
对于反应CO2(g)+H2(g)  CO(g)+H2O(g) ΔH>0,在其他条件不变的情况下( )
CO(g)+H2O(g) ΔH>0,在其他条件不变的情况下( )
| A.加入催化剂,改变了反应的速率,反应的ΔH也随之改变 |
| B.降低温度,反应速率加快,反应放出的热量不变 |
| C.改变反应体系体积,平衡不发生移动,反应放出的热量不变 |
| D.若将上述反应改为在燃料电池进行,反应放出的热量不变 |
下列离子方程式与所述事实相符且正确的是( )
A.向明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO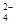 +2Ba2++4OH-===2BaSO4↓+AlO +2Ba2++4OH-===2BaSO4↓+AlO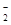 +2H2O +2H2O |
| B.稀HNO3溶液与难溶于水的FeS固体:FeS+2H+===Fe2++H2S↑ |
C.碳酸氢镁与少量澄清石灰水反应:Ca2++2OH-+2HCO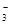 ===CaCO3↓+CO ===CaCO3↓+CO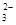 +2H2O +2H2O |
D.强碱溶液中,次氯酸钠与Fe(OH)2:3ClO-+2Fe(OH)2===2FeO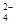 +3Cl-+H2O+4H+ +3Cl-+H2O+4H+ |
下列有关实验的描述或操作错误的是()
| A.牙膏中含有不溶于水的成分,如碳酸钙、磷酸钙、氢氧化铝、二氧化硅等,它们主要做摩擦剂 |
| B.纸上层析法通常以滤纸作为惰性支持物。滤纸纤维上的羟基具有亲水性,它所吸附的水作为固定相。 |
| C.欲检验火柴头燃烧后的气体中是否含有SO2,可将燃烧后气体通入KMnO4酸性溶液,观察KMnO4溶液颜色是否变浅或褪色。 |
| D.减压过滤可以用于过滤胶状沉淀或颗粒太小的沉淀。 |
铝和镓的性质相似,如M(OH)3都是难溶的两性氢氧化物。在自然界镓常以极少量分散于铝矿中。用NaOH溶液处理铝矿(Al2O3)时,生成NaAlO2、NaGaO2;而后通入适量CO2,得Al(OH)3沉淀,而NaGaO2留在溶液中(循环多次后成为提取镓的原料)。发生后一步反应是因为
| A.铝酸酸性弱于镓酸 | B.铝酸酸性强于镓酸 |
| C.NaGaO2浓度小,不沉淀 | D.Al(OH)3是难溶物 |
室温下,强酸性和强碱性溶液中都不能共存的离子组是
| A.NH4+、Cu2+、SO42-、NO3- | B.K+、Na+、SO32-、S2- |
| C.K+、Na+、Al3+、SO42- | D.Mg2+、Fe2+、NO3-、I- |