锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成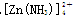 。
。
回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为________(用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式
________________________________________________________________________。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是________。
①硫酸铝和氢氧化钠 ②硫酸铝和氨水 ③硫酸锌和氢氧化钠 ④硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式
________________________________________________________________________。
试解释在实验室不适宜用可溶性锌盐与氨水反应制备Zn(OH)2的原因
________________________________________________________________________。
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子 Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是和_______(填化学式)。
(2)为了确定X,现将(1)中的两种物质记为A和B,含X的物质记C,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生棕黄色沉淀,向该沉淀中滴人稀硝酸沉淀部分溶解,最后留有白色沉淀不再溶解。则X为____。
A.SO32-B.SO42-C.CH3COO-D.SiO32-
(3)B的水溶液显___性,原因为____。(用离子方程式表示)
(4)将0. 02 molA与0.0 1molC同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的质量为________(保留一位小数)。
(5)将Cu投人到装有D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的_____(填相应的离子符号)。有关反应的离子方程式为:____________。
(6)利用上述已经确定的物质,可以检验出D、E中的阳离子。请简述实验操作步骤、现象及结论_________________。
向含有a mol FeBr3的溶液中,加入x mol Na2S。
A.当2x=a时,离子方程式为____________。
B.当x=a时,离子方程式为____________。
(1)含10.8gAl3+的Al2(SO4)3中所含的SO42-的物质的量是。
(2)已知16g A与20g B恰好完全反应生成0.04 mol C和31.76g D,则C的摩尔质量为。
(3)0.1 mol Na中含mol e-,在跟足量水反应中失去mol e-。
(4)标准状况下V L氨气溶解在1L水中,所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为c mol/L,则ω=。
根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示)
(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式:。
(2)某同学取X的溶液,酸化后通入氧气再加入KI、淀粉溶液,变为蓝色,写出与上述变化过程相关的离子方程式:、。
(3)写出Cl2将Z氧化为K2EO4的化学方程式:。
氧化还原反应中实际上包含氧化和还原两个过程,下面是一个还原过程的半反应式:2NO3-+10H++8e-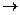 N2O+5H2O
N2O+5H2O
Fe2(SO4)3、KmnO4、Na2CO3、FeSO4四种物质中的一种物质能使上述还原过程发生。
(1)写了并配平该氧化还原反应的化学方程式:。
(2)该反应中氧化剂和还原剂物质的量之比为。
(3)反应中硝酸体现了、性质。
(4)反应中若产生0.1mol气体(N2O),则转移电子的物质的量是。