Ⅰ、乙烷、乙烯、乙炔、乙苯四种有机物中具有下列性质的是
(1) 不能使溴水因反应而褪色,但能使酸性高锰酸钾溶液褪色的是________。
(2)既不能使溴水褪色,也不能使酸性高锰酸钾溶液褪色的是__________。与之互为同系物且相对分子质量相差14的有机物的分子式为__________、__________。
(3)在催化剂作用下能与氢气按1:2完全反应的是___________。
(4)该物质一定条件下能与水反应生成酒精的,写出发生反应的化学方程式_______________________________________,反应类型为: 。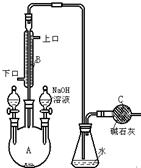
Ⅱ、制备溴苯的实验装置如右图所示,回答下列问题:
(1)写出制取溴苯的反应方程式为 。
(2)将左侧分液漏斗的旋塞打开滴入试剂后开始反应,在A中可观察到的现象是 。
(3)冷凝管B有上口和下口,冷却水应从 口进入。
(4)反应结束后将右侧分液漏斗中的物质在加入A中,其作用是(用化学方程式回答) 。
(5)要证明该反应是取代反应,简便的实验方法是 _____________________
____________________________________________ 。(写出操作、现象、结论)
在某无色溶液中,加入盐酸酸化的BaCl2溶液有白色沉淀,则下列判断正确的是
| A.一定有SO42- | B.可能有SO42-或Ag+ |
| C.一定有Ag+ | D.可能有SO32-或SO42- |
下列各组气体中,在通常状况下能共存,并且都能用浓硫酸干燥的是
| A.SO2、H2S、Cl2 | B.SO2、O2、NH3 |
| C.SO2、CO2、O2 | D.HCl、H2S、HI |
检验试管中盛有的少量白色固体是铵盐的方法是
| A.将固体加热,用湿润的红色石蕊试纸在试管口检验,看是否变蓝 |
| B.加水溶解,用pH试纸测溶液的酸碱性 |
| C.加入NaOH溶液,加热,再滴入酚酞试液 |
| D.加入NaOH溶液,加热,用湿润的红色石蕊试纸在试管口检验,看是否变蓝 |
下列电子式正确的是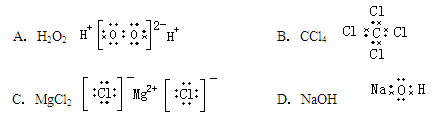
下列有关酸雨的说法正确的是
| A.酸雨就是指pH<7的雨水 |
| B.酸雨是因为雨水中含有CO2 |
| C.工业上大量燃烧含硫燃料和以含硫矿石为原料冶炼金属产生的SO2是产生硫酸型酸雨的主要原因 |
| D.酸雨没有危害,所以不必担心,也不必想办法治理 |