在一体积为2 L的密闭容器中加入反应物A、B,发生如下反应:
A+2B 3C。反应经2 min后,A的浓度从开始时的1.0 mol/L 降到0.8 mol/L。
3C。反应经2 min后,A的浓度从开始时的1.0 mol/L 降到0.8 mol/L。
已知反应开始时B的浓度是1.2 mol/L。则:
(1)2 min末B的浓度 。
(2) 2 min内 ,用A物质的浓度变化来表示该反应的反应速率,即v(A)= 。
根据烷、烯、炔烃燃烧的反应方程式,有人总结出以下规律:
对于烷烃有:n(烷烃)=n(H2O)−n(CO2),对于烯烃有n(H2O)−n(CO2)=0,对于炔烃有
n(炔烃)=n(CO2)−n(H2O)。请回答下列问题:
(1)某混合气体由C2H6和C3H4组成。将1.0L混合气在氧气中充分燃烧,产生的CO2体积比水蒸气多0.2L(相同状况下测定),通过计算确定C2H6的体积。(请写出计算过程)
(2)某混合气由烯烃和烷烃或烯烃和炔烃组成。组成中可能是两种气体,也可能是多种气体。将1.0L混合气在氧气中充分燃烧,产生3.0LCO2和2.4L水蒸气(相同状况下测定)。试判断混合气是由烯烃和两类烃组成,其体积比为。
下图是100 mg CaC2O4·H2O受热分解时,所得固体产物的质量随温度变化的曲线。试利用图中信息结合所学的知识填空: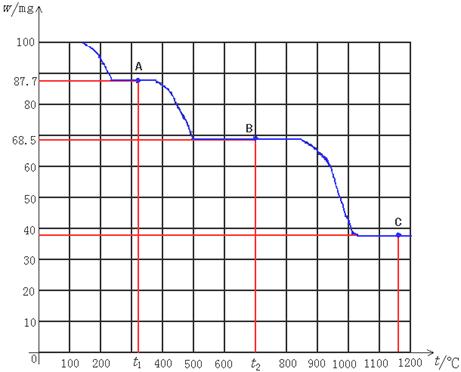
(1)温度分别为t1和t2时,固体产物的化学式A是________,B是________。产物C的化学式为。
(2)由A得到B的化学方程式为___________________________________。
(8分) 25℃时,若体积为Va、pH=a 的某一元强酸与体积为Vb、pH=b的某一元强碱混合,恰好中和,且已知Va>Vb和a=0.5b。则:
(1) a值可否等于3 (填“可”或“否”),其理由是。
(2) a值可否等于5(填“可”或“否”),其理由是。
(3)a 的取值范围。
某抗酸药每片含碳酸钙534 mg、氢氧化镁180 mg。试计算10片该药片理论上可与1. 00 mol·L-1的盐酸溶液多少毫升完全反应?
(6分)臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧:3O22O3。
(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为多少?(保留一位小数)。
(2)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧的体积为多少升?
(3)实验室将氧气和臭氧的混合气体0.896 L(标准状况)通入盛有20.0 g铜粉的反应器中,充分加热后,粉末的质量变为21.6 g。则原混合气中臭氧的体积分数为多少?